题目内容
12.某200mL Fe2(SO4)3溶液中含有0.1molFe3+,该溶液中SO42-的物质的量浓度为( )| A. | 0.75mol/L | B. | 0.5mol/L | C. | 1mol/L | D. | 0.25mol/L |
分析 由Fe2(SO4)3可知,Fe3+、SO42-的物质的量比为2:3,结合c=$\frac{n}{V}$计算.
解答 解:由Fe2(SO4)3可知,Fe3+、SO42-的物质的量比为2:3,含有0.1molFe3+,则含SO42-的物质的量为0.1mol×$\frac{3}{2}$=0.15mol,该溶液中SO42-的物质的量浓度为$\frac{0.15mol}{0.2L}$=0.75mol/L,故选A.
点评 本题考查物质的量浓度的计算,为高频考点,把握物质的量与浓度的关系为解答的关键,侧重分析与计算能力的考查,注意物质的构成,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列关于氮元素相关物质叙述正确的是( )
| A. | 铵盐中氮元素都是-3价 | |
| B. | 铵盐加热分解后都有NH3生成 | |
| C. | 氨的催化氧化反应属于人工固氮过程 | |
| D. | 氮氧化物是形成酸雨的来源之一 |
3.做氯化氢喷泉实验后,烧瓶内的液体只占烧瓶容积的三分之一,其原因可能是( )
| A. | HCl气体没有完全溶解 | B. | 装置漏气,进入空气 | ||
| C. | 集气时有空气混入 | D. | 从胶头滴管挤入烧瓶的水太少 |
7.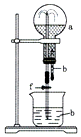 在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )
在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )
 在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( )
在如图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是( ) | a(干燥气体) | b(液体) | |
| A | NO2 | 水 |
| B | CO2 | CaCl2溶液 |
| C | Cl2 | 饱和NaCl溶液 |
| D | NH3 | 水 |
| A. | A | B. | B | C. | C | D. | D |
17.下列反应属于取代反应的是( )
| A. | 乙酸乙酯在酸性条件下水解 | B. | 乙炔使溴的四氯化碳溶液褪色 | ||
| C. | 由乙醇制乙烯 | D. | 甲苯使酸性KMnO4溶液褪色 |
4.下列属于电解质的是( )
| A. | 酒精 | B. | 石灰水 | C. | 碳酸钠 | D. | 铁 |
1.下列说法不正确的是( )
| A. | 一水合氨的电离方程式:NH3•H2O?NH4++OH- | |
| B. | 氯化镁的摩尔质量:95g | |
| C. | 亚硫酸的化学式:H2SO3 | |
| D. | Na+的结构示意图: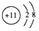 |