题目内容
6.废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废旧干电池的糊状物{二氧化锰、碳粉、淀粉[化学式(C6H10O5)n]、氯化铵和氯化锌等}从中回收并得到纯净的二氧化锰.需经过溶解、过滤、干燥及灼烧等步骤.(1)溶解时,需要用到的玻璃仪器有烧杯、玻璃棒(2)若发现过滤时,滤液浑浊,可能的原因有滤纸破裂、加入混合液超出滤纸边缘(写出两点).
(3)洗涤时.洗涤沉淀及如何证明已洗涤干净的方法为在过滤器中加入蒸馏水,至没过固体,静置,使其自然流下,重复2-3次;取最后一次洗涤滤液,向其中加入硝酸银溶液,若没有白色沉淀出现,则说明已经洗涤干净,否则就没洗涤干净
(4)在空气中灼烧时,用到三脚架、泥三角,坩埚钳,还用到仪器有坩埚灼烧时碳粉转变为CO2(写化学式)
(5)若二氧化锰干燥后未灼烧,能否用作氯酸钾分解制氧气的催化剂,并说明理由不能,二氧化锰中会含有碳及一些未溶解的有机物与氧气反应,发生危险.
分析 (1)根据溶解操作可判断实验需要用到的玻璃仪器;
(2)过滤时,滤纸破裂、加入混合液超出滤纸边缘等都会导致滤液浑浊;
(3)洗涤时主要除去废旧干电池的糊状物中的氯化物,洗涤沉淀的方法同过滤操作,判断已洗涤干净主要是根据洗涤滤液中是否有氯离子存在;
(4)灼烧固体要在坩埚中进行,在空气中灼烧时碳粉会转变为CO2;
(5)若二氧化锰干燥后未灼烧,则其中会含有碳及一些未溶解的有机物,在用这样的二氧化锰作催化剂制氧气时会与氧气反应,发生危险.
解答 解:(1)根据溶解操作可知,实验需要用到的玻璃仪器有烧杯、玻璃棒,
故答案为:烧杯、玻璃棒;
(2)过滤时,滤纸破裂、加入混合液超出滤纸边缘等都会导致滤液浑浊,
故答案为:滤纸破裂、加入混合液超出滤纸边缘;
(3)洗涤时主要除去废旧干电池的糊状物中的氯化物,洗涤时,在过滤器中加入蒸馏水,至没过固体,静置,使其自然流下,重复2-3次;判断已洗涤干净的方法是取最后一次洗涤滤液,向其中加入硝酸银溶液,若没有白色沉淀出现,则说明已经洗涤干净,否则就没洗涤干净,
故答案为:在过滤器中加入蒸馏水,至没过固体,静置,使其自然流下,重复2-3次;取最后一次洗涤滤液,向其中加入硝酸银溶液,若没有白色沉淀出现,则说明已经洗涤干净,否则就没洗涤干净;
(4)灼烧固体要在坩埚中进行,在空气中灼烧时碳粉会转变为CO2,
故答案为:坩埚;CO2;
(5)若二氧化锰干燥后未灼烧,则其中会含有碳及一些未溶解的有机物,在用这样的二氧化锰作催化剂制氧气时会与氧气反应,发生危险,所以若二氧化锰干燥后未灼烧,则不能否用作氯酸钾分解制氧气的催化剂,
故答案为:不能,二氧化锰中会含有碳及一些未溶解的有机物与氧气反应,发生危险.
点评 本题主要考查实验室废弃旧电池中回收并得到纯净的二氧化锰,考查学生对实验基本操作的掌握情况,熟练掌握实验的基本操作是解答的关键,平时注意打好扎实的基础知识和灵活应用知识解决问题的能力培养,题目难度中等.

| A. | 二氧化碳的结构式:O-C-O | B. | 羟基的电子式为: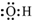 | ||
| C. | 丙烷分子的球棍模型: | D. | 硫离子的结构示意图: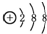 |
| A. | ①②⑤ | B. | ②④ | C. | ②③⑤ | D. | 只有④ |
| A. | 称量NaOH固体时,放在烧杯中且称量较慢 | |
| B. | 定容时,俯视刻度线 | |
| C. | 定容时,加水超过刻度线,再用胶头滴及将过线的液体吸出 | |
| D. | 移液前,容量瓶中有少量蒸馏水 |
| A. | ②④⑦ | B. | ①③④ | C. | ②④⑥ | D. | ④⑥⑦ |
| A. | 混合溶液的pH等于7 | B. | 混合溶液的pH大于7 | ||
| C. | 加入酸碱的物质的量相等 | D. | 混合溶液还能再中和盐酸 |
| A. | 过滤,可以除去NaCl溶液中少量的淀粉胶体 | |
| B. | 溶解、过滤,可以提纯含少量BaSO4的BaCO3 | |
| C. | 加热蒸发,可以除去粗盐中的CaCl2、MgCl2等杂质 | |
| D. | 加入足量铁屑,充分反应后,过滤,可以除去FeCl2溶液中少量FeCl3 |
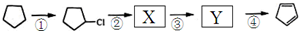

 (任写一种).金刚烷与四氢二聚环戊二烯的关系是B.(填字母)
(任写一种).金刚烷与四氢二聚环戊二烯的关系是B.(填字母)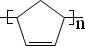 ..
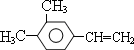
.. .请写出下列反应的有机产物的结构简式:
.请写出下列反应的有机产物的结构简式: OHC-CHO、OHC-CH2-CHO.
OHC-CHO、OHC-CH2-CHO.