题目内容
1.硅及其化合物在材料领域中应用广泛.下列叙述中,正确的是( )| A. | 硅酸盐是良好的半导体材料 | B. | 硅是地壳中含量最多的元素 | ||
| C. | SiO2不溶于水,也不溶于任何酸 | D. | 二氧化硅用于制作光导纤维 |
分析 A.晶体硅可作半导体材料;
B.氧是地壳中含量最多的元素;
C.SiO2不溶于水,但能溶于氢氟酸;
D.光导纤维的主要成分是二氧化硅.
解答 解:A.晶体硅是良好的半导体材料,故A错误;
B.氧是地壳中含量最多的元素,硅仅次于氧,故B错误;
C.SiO2不溶于水,但能溶于氢氟酸,二氧化硅能和氢氟酸反应生成四氟化硅,故C错误;
D.二氧化硅是生产光导纤维的主要原料,故D正确;
故选:D.
点评 本题考查硅和二氧化硅的性质,题目难度不大,注意基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.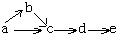 a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价
a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价
氧化物对应水化物,且是一种强电解质,则a可能是( )
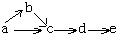 a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价
a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价氧化物对应水化物,且是一种强电解质,则a可能是( )
| A. | N2 | B. | C12 | C. | Si | D. | C |
6.NA代表阿伏加德罗常数.下列有关NA的叙述中,不正确的是( )
| A. | 1 mol 任何气体所含的分子数均为NA | |
| B. | 14 g氮气所含的氮原子数为NA | |
| C. | 标准状况下,22.4 L水所含的水分子数为NA | |
| D. | 在钠与氯气的反应中,1 mol钠失去电子的数目为NA |
13.在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的关系如表:
①试判断K1>K2(填写“>”,“=”或“<”)
②下列各项能说明该反应已达到平衡状态的是c(填字母)
a.单位时间内,消耗1molN2的同时生成2mol NH3 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变.
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②下列各项能说明该反应已达到平衡状态的是c(填字母)
a.单位时间内,消耗1molN2的同时生成2mol NH3 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变.
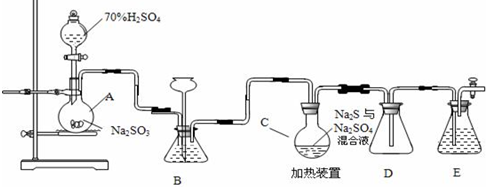
11.在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:

(1)A装置中所发生反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O.C装置中稀硫酸的作用为:吸收从B装置中的试管内逸出.
(2)表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
参照表中数据,请分析B装置中使用冰水是因为温度越低,碳酸氢钠的溶解度越小,便于析出.
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在A与B装置之间(填写字母)连接一个盛有饱和NaHCO3溶液的洗气装置,其作用是除去CO2中混合的HCl气体.
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为60%.

(1)A装置中所发生反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O.C装置中稀硫酸的作用为:吸收从B装置中的试管内逸出.
(2)表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在A与B装置之间(填写字母)连接一个盛有饱和NaHCO3溶液的洗气装置,其作用是除去CO2中混合的HCl气体.
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为60%.