题目内容
14.下列对相关实验操作的说法中,一定正确的是( )| A. | 实验室配制480 mL 0.1 mol/L NaOH溶液,需要准确称量NaOH 1.920 g | |
| B. | 学生实验测定硫酸铜晶体中结晶水含量时,通常至少称量4次 | |
| C. | 酸碱中和滴定实验中只能用标准液滴定待测液 | |
| D. | 分液时,分液漏斗中下层液体从下口放出后,换一容器再从下口放出上层液体 |
分析 A.配制480 mL 0.1 mol/L NaOH溶液,选择500mL容量瓶,结合m=nVM计算;
B.实验测定加热前后固体的质量,且直至连续两次称量的差不超过0.1 g为止;
C.中和滴定实验中氢离子的物质的量与氢氧根离子的物质的量相等;
D.分液时,避免上下层液体混合.
解答 解:A.配制480 mL 0.1 mol/L NaOH溶液,选择500mL容量瓶,NaOH的质量m=nVM=0.5L×0.1mol/L×40g/mol=2.0g,故A错误;
B.在硫酸铜结晶水含量的测定实验中,实验中的加热、冷却、称量的操作步骤要重复进行,直至连续两次称量的差不超过0.1 g为止,一般情况下,结晶水含量测定时称量次数不得少于4次,故B正确;
C.中和滴定实验中氢离子的物质的量与氢氧根离子的物质的量相等,则可以利用标准液滴定待测液,也可利用待测液滴定标准液,故C错误;
D.分液时,避免上下层液体混合,则分液漏斗中下层液体从下口放出后,上层液体从上口倒出,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握溶液配制、结晶水测定实验、中和滴定及混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.

练习册系列答案
相关题目
4.配制100mL 0.01mol•L-1KOH溶液时,必须用到的仪器是( )
| A. | 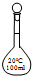 100mL容量瓶 100mL容量瓶 | B. |  100mL集气瓶 | C. | 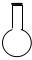 100mL烧瓶 | D. |  100mL滴瓶 100mL滴瓶 |
5.饱和二氧化硫水溶液中存在下列平衡体系:
SO2+H2O?H++HSO3-
HSO3-?H++SO3-
若向此溶液中( )
SO2+H2O?H++HSO3-
HSO3-?H++SO3-
若向此溶液中( )
| A. | 加水,SO3-浓度增大 | |
| B. | 通入少量Cl2气体,溶液pH增大 | |
| C. | 加少量CaSO3粉末,HSO3-浓度基本不变 | |
| D. | 通入少量HCl气体,溶液中HSO3-浓度减小 |
9.下列操作不正确的是( )
| A. | 配制氯化铁溶液时需加入少量盐酸 | |
| B. | 金属钠保存在装有煤油的带玻璃塞的广口瓶中 | |
| C. | 保存液溴需用水封,放在带橡皮塞子的棕色细口瓶中 | |
| D. | 用稀硝酸洗去附在试管内壁的银镜 |
19.在100g浓度为ω%的稀硫酸中加入4g氧化铜粉末,待氧化铜全部溶解后,向所得蓝色溶液中加入10g铁粉,充分反应后,过滤,得滤液和4.8g滤渣.下列计算结果正确的是( )
| A. | 4.8g滤渣是由3.2g铜和1.6g铁组成 | B. | ω=14.7 | ||
| C. | 反应过程中产生的氢气是2.24L | D. | 滤液是20.88%的硫酸亚铁溶液 |
6.由分类思想,下列说法正确的是( )
| A. | 氢氧化钠、盐酸都为强电解质 | |
| B. | 铁生锈、食物腐败都有氧化反应发生 | |
| C. | 糖类、蛋白质都为高分子化合物 | |
| D. | 一氯甲烷、二氧化碳都是极性分子 |
3.模拟电渗析法将海水淡化的工作原理示意图如下.已知X、Y均为惰性电极,模拟海水中富含Na+、Cl-、Ca2+、Mg2+、SO42-、HCO3-等离子.下列叙述中正确的是( )


| A. | M是阴离子交换膜 | B. | Y电极上产生无色气体 | ||
| C. | X电极区域可产生Mg(OH)2 | D. | X电极反应式为4OH--4e-═O2↑+2H2O |
4.汽车已经进入千家万户,汽油来自于石油化工.下列说法不正确的是( )
| A. | 石油中含有1~50个碳原子的烷烃及环烷烃 | |
| B. | 石油分馏是物理变化,裂化、裂解和催化重整属于化学变化 | |
| C. | 石油裂化的目的主要是提高汽油的产量 | |
| D. | 裂化主要是将链烃变为芳香烃 |
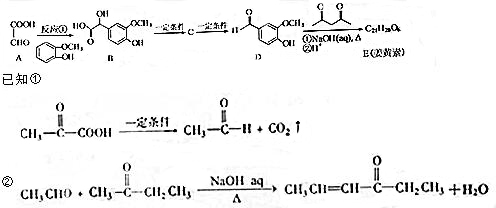
 .
.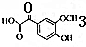 .
.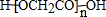 .
. ,下列有关E的叙述正确的是ac.
,下列有关E的叙述正确的是ac.