题目内容
4.金刚烷是一种重要的化工原料,分子式为C10H16,结构为: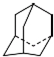 ,用一个氯原子与一个溴原子取代后形成的二元取代物数目为( )
,用一个氯原子与一个溴原子取代后形成的二元取代物数目为( )| A. | 8 | B. | 7 | C. | 6 | D. | 5 |
分析 判断分子中氢原子的环境,烃的二卤代物的同分异构体可以采用固定1个卤素原子移动另1个卤素原子的方法进行确定.
解答 解:分子中含4个CH,6个CH2,共2种位置的H,氯定在单氢碳原子上时,溴的位置有三种(邻、间、对)即有三种同分异构体;氯定在双氢碳原子上时,溴的位置有五种(同、邻、间、间二、间三)即有五种同分异构体,(间指氯与溴所连碳原子之间间隔一个碳原子,间二指氯与溴所连碳原子之间间隔二个碳原子,间三指氯与溴所连碳原子之间间隔三个碳原子)如图所示:数字代表溴原子位置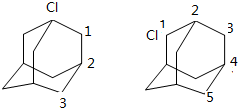 ,故选A.
,故选A.
点评 本题主要考查了同分异构体的判断,题目难度中等,注意判断等效氢的种类.

练习册系列答案
相关题目
14.与乙烯所含碳、氢元素的质量分数相同,但与乙烯既不是同系物又不是同分异构体的是( )
| A. | 环丙烷(C3H6) | B. | 乙烷 | C. | 甲烷 | D. | 丙烯(CH3CH═CH2) |
15.下列有关几种常见的金属和非金属及其化合物的说法正确的是( )
| A. | Na、Mg、Al、Fe、Cu都能导电,它们的氧化物都能与酸反应 | |
| B. | 铝热反应是指铝能将所有的金属从其氧化物中置换出来 | |
| C. | CO2、NO、SO2都是非金属氧化物,都属于酸性氧化物 | |
| D. | CaCO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸 |
12.根据下列事实所作的结论,正确的是( )
| 编号 | 事实 | 结论 |
| A | 不存在两种邻二甲苯 | 苯分子中碳碳键完全相同,而不是单双键交替结构 |
| B | 最简式相同的烃 | 要么是同系物要么是同分异构体 |
| C | 质量相同的甲、乙两种有机物完全燃烧时产生质量相同的水 | 甲、乙两种分子中,各元素的原子个数比一定相同 |
| D | 甲、乙两种有机物具有相同相对分子质量和不同结构 | 甲和乙一定是同分异构体 |
| A. | A | B. | B | C. | C | D. | D |
19.某同学用中和滴定的方法测定混有少量Na2CO3的NaOH固体中NaOH的含量,准确称取2.0g样品配制成200mL溶液,然后分三次各取20.00mL溶液于三个洁净的锥形瓶中,分别加入过量BaCl2溶液和1~2滴指示剂,用浓度为0.2000mol•L-1的盐酸标准液进行滴定.
(1)滴定时应选用酚酞作指示剂;到达滴定终点的实验现象是最后一滴盐酸滴入后,溶液由浅红色变为无色且30秒不改变.
(2)下列操作会导致烧碱样品中NaOH含量测定值偏高的是BC.
A.锥形瓶未用待测液润洗
B.酸式滴定管未用标准液润洗
C.在滴定前有气泡,滴定后气泡消失
D.滴定前平视读数,滴定结束俯视读数
E.滴定终点前加水清洗锥形瓶
F.指示剂变色后立即读数
(3)实验相关数据记录如下:
依据表中数据,计算样品中NaOH的质量分数80%.
(1)滴定时应选用酚酞作指示剂;到达滴定终点的实验现象是最后一滴盐酸滴入后,溶液由浅红色变为无色且30秒不改变.
(2)下列操作会导致烧碱样品中NaOH含量测定值偏高的是BC.
A.锥形瓶未用待测液润洗
B.酸式滴定管未用标准液润洗
C.在滴定前有气泡,滴定后气泡消失
D.滴定前平视读数,滴定结束俯视读数
E.滴定终点前加水清洗锥形瓶
F.指示剂变色后立即读数
(3)实验相关数据记录如下:
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.60 | 20.62 |
| 2 | 20.00 | 0.80 | 20.78 |
| 3 | 20.00 | 0.20 | 20.90 |
9.下列单质或化合物的描述正确的是( )
| A. | 明矾溶于水产生具有吸附性的胶体粒子,可作漂白剂 | |
| B. | 植物油分子中有碳碳双键,与H2加成后可以得到人造脂肪 | |
| C. | CO2、CH4、N2等均是造成温室效应的气体 | |
| D. | Fe在少量Cl2中燃烧生成FeCl2 |
16.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 等质量的H2O与CH2D2含有的质子数相同 | |
| B. | 室温下向1 L pH=1的醋酸溶液中加水,所得溶液中H+数目大于0.1NA | |
| C. | 常温下1 L 0.5mol•L-1NH4Cl溶液与2L 0.25mol•L-1NH4Cl溶液所含NH4+的数目相同 | |
| D. | 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.4NA |
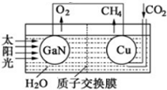 氮化镓是目前最热门的半导体材料,应用前景非常广阔.已有科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4,装置如图所示,回答下列问题:
氮化镓是目前最热门的半导体材料,应用前景非常广阔.已有科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4,装置如图所示,回答下列问题: