题目内容
已知下列两个热化学方程式
2H2(g)+O2(g)=2H2O(1) △H= -571.6KJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0kJ/mol
实验测得,5mol氢气和丙烷的混合气体完全燃烧时放热3847kJ,则混合气体中氢气与丙烷的体积比是
A.1:3 B.3:1 C.1:4 D.1:1
B
【解析】
试题分析:1mol混合气体完全燃烧放热3847kJ/5=769.4kJ,根据十字交叉法,氢气与丙烷的体积比(2220.0-769.4):(769.4-571.6/2)=3:1,答案选B。
考点:热化学方程式的计算

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
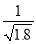 ×10-11 mol·L-1
×10-11 mol·L-1
 2 H2O+O2↑中每生成1mol O2转移的电子数为NA
2 H2O+O2↑中每生成1mol O2转移的电子数为NA