��Ŀ����
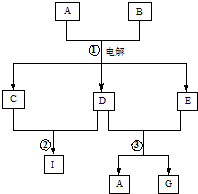 ����ͼ��ʾ������ת����ϵ�У�A�Ǻ�ˮ�к�����ḻ���Σ�B�dz�������ɫҺ�壬G��ˮ��Һ��һ�ֳ��õ�Ư��������Ӧ�����ɵ�ˮ�Ͳ��ַ�Ӧ����δ�г���
����ͼ��ʾ������ת����ϵ�У�A�Ǻ�ˮ�к�����ḻ���Σ�B�dz�������ɫҺ�壬G��ˮ��Һ��һ�ֳ��õ�Ư��������Ӧ�����ɵ�ˮ�Ͳ��ַ�Ӧ����δ�г�����1������A�������ӵĽṹʾ��ͼ��
��2����Ӧ���ڵ�ȼ�����µ������ǣ�
��3����Ӧ�ٵĻ�ѧ����ʽΪ��
��4����ҵ�Ʊ�Ư�۵Ļ�ѧ����ʽΪ��
��Ч�ȵĺ����Ǻ�����������������������Ҫָ�꣮�������ε���Ч�Ⱥ������ô������������ᷴӦ�����ɵ������ĺ�������ʾ��ClO-+Cl-+2H+=Cl2��+H2O
��Ч�Ⱥ���=
| m(Cl2) |
| m(��������) |
���㣺������ƶ�
ר�⣺
������A�Ǻ�ˮ�к�����ḻ���Σ���AΪNaCl��B�dz�������ɫҺ�壬���A��B����C��D��E��������֪BΪH2O����D��E��Ӧ����A��NaCl����G��G��ˮ��Һ��һ�ֳ��õ�Ư��������֪GΪNaClO���÷�Ӧ��������NaOH��Ӧ����CΪH2��D������������������Ӧ����DΪCl2��EΪNaOH������֪IΪHCl���ݴ˽��
���
�⣺A�Ǻ�ˮ�к�����ḻ���Σ���AΪNaCl��B�dz�������ɫҺ�壬���A��B����C��D��E��������֪BΪH2O����D��E��Ӧ����A��NaCl����G��G��ˮ��Һ��һ�ֳ��õ�Ư��������֪GΪNaClO���÷�Ӧ��������NaOH��Ӧ����CΪH2��D������������������Ӧ����DΪCl2��EΪNaOH������֪IΪHCl��
��1��AΪNaCl���������ӵĽṹʾ��ͼΪ��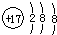 ���ʴ�Ϊ��
���ʴ�Ϊ��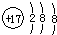 ��
��
��2����Ӧ����������������ȼ�գ������ǣ�����ȼ�ա���ɫ���桢�����������ʴ�Ϊ������ȼ�ա���ɫ���桢����������
��3����Ӧ�ٵĻ�ѧ����ʽΪ��2NaCl+2H2O
Cl2��+H2��+2NaOH���ʴ�Ϊ��2NaCl+2H2O
Cl2��+H2��+2NaOH��
��4����ҵ�Ʊ�Ư�۵Ļ�ѧ����ʽΪ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O������������Ϊ1mol������2molClO-����ClO-+Cl-+2H+=Cl2��+H2O��֪����������Ϊ2mol����������������Ϊ2mol��71g/mol=142g��Ư�۵�����Ϊ1mol��111g/mol+1mol��143g/mol=254g���ʸ÷�Ӧ�IJ�ƷƯ�۵���Ч��Ϊ
��100%=55.9%��
�ʴ�Ϊ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��55.9%��
��1��AΪNaCl���������ӵĽṹʾ��ͼΪ��
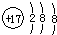 ���ʴ�Ϊ��
���ʴ�Ϊ��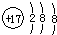 ��
����2����Ӧ����������������ȼ�գ������ǣ�����ȼ�ա���ɫ���桢�����������ʴ�Ϊ������ȼ�ա���ɫ���桢����������
��3����Ӧ�ٵĻ�ѧ����ʽΪ��2NaCl+2H2O
| ||
| ||
��4����ҵ�Ʊ�Ư�۵Ļ�ѧ����ʽΪ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O������������Ϊ1mol������2molClO-����ClO-+Cl-+2H+=Cl2��+H2O��֪����������Ϊ2mol����������������Ϊ2mol��71g/mol=142g��Ư�۵�����Ϊ1mol��111g/mol+1mol��143g/mol=254g���ʸ÷�Ӧ�IJ�ƷƯ�۵���Ч��Ϊ
| 142g |
| 254g |
�ʴ�Ϊ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��55.9%��
���������⿼�������ƶϣ��漰�ȼҵ�ȣ��ѶȲ���ע��Ի���֪ʶ��ȫ�����գ���4���м���Ϊ�״��㣬ע�����Ư�۵���Ч�ȣ�ѧ��������������ε���Ч�ȣ�

��ϰ��ϵ�д�
 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
�����Ŀ
��֪H-H����Ϊ436KJ/mol��H-N����Ϊ391KJ/mol�����ݻ�ѧ����ʽN2+3H2=2NH3��H=-92.4KJ/mol����N��N���ļ����ǣ�������
| A��431 KJ/mol |
| B��946 KJ/mol |
| C��649 KJ/mol |
| D��869 KJ/mol |
ij��ɫ����ǿ������Һ���ܴ���������������ǣ�������
| A��Na+ Cu2+ NO3- Cl- |
| B��K+ NO3- Na+Cl- |
| C��K+ CO32- NO3- Ca2+ |
| D��K+ NO3- SO42- Mg2+ |
�����ˮ������CN-�о綾����������±���������ƣ���ԭ�Խ���I-��Br-֮�䣬HCNΪ���ᣮ����˵������ȷ���ǣ�������
| A��CN-���Ժ�ϡ���ᷴӦ����HCN |
| B��CN-�ɱ�Cl2�����ɣ�CN��2 |
| C����ˮ��Һ�У�CN��2�ɱ�F-��ԭ |
| D��HCN�ĽṹʽΪ H-C��N |
�����������Ļ���ﹲa mol����һ������������ȫ���ܽ⣬�õ�����Һ�в���Fe3+��ͬʱ�ռ���b mol��������ԭ������������������ʵ���Ϊ��������
A��
| ||
B��
| ||
| C����a-b��mol | ||
| D��b mol |