题目内容
7.Ni2+与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验Ni2+.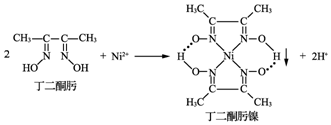
(1)Ni2+基态核外电子排布式为1s22s22p63s23p63d8或[Ar]3d8.
(2)1mol丁二酮肟分子中含有σ键的数目为15mol.
(3)丁二酮肟镍分子中碳原子的杂化轨道类型为sp3和sp2.
(4)Ni(CO)4是一种无色液体,沸点为43℃,熔点为-19.3℃.Ni(CO)4的晶体类型是分子晶体.
(5)与CO互为等电子体的二价阴离子为C22-,Ni(CO)4中Ni与CO的C原子形成配位键,不考虑空间构型,Ni(CO)4的结构可用示意图表示为
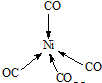 .
.
分析 (1)镍原子核外电子数是28,镍原子失去最外层2个电子变成基态Ni2+,根据构造原理书写基态Ni2+的核外电子排布式;
(2)单键中含有一个σ键,双键含有一个σ键和一个π键;
(3)根据价层电子对互斥理论确定中心原子杂化方式;
(4)分子晶体的熔沸点较低;
(5)价电子数相等、原子个数相等的微粒为等电子体;Ni(CO)4中Ni与CO的C原子形成配位键,形成四面体结构.
解答 解:(1)镍原子核外电子数是28,镍原子失去最外层2个电子变成基态Ni2+,根据构造原理知,基态Ni2+的核外电子排布式为1s22s22p63s23p63d8(或[Ar]3d8),故答案为:1s22s22p63s23p63d8(或[Ar]3d8);
(2)已知丁二酮肟的结构式为 ,分子中含有13个单键,和2个双键,则共含有15个σ键,所以1mol丁二酮肟含有σ键数目为15mol;
,分子中含有13个单键,和2个双键,则共含有15个σ键,所以1mol丁二酮肟含有σ键数目为15mol;
故答案为:15;
(3)甲基上碳原子价层电子对个数是4且不含孤电子对,为sp3杂化,连接甲基的碳原子含有3个价层电子对且不含孤电子对,为sp2杂化,
故答案为:sp3和sp2;
(4)分子晶体的熔沸点较低,所以该物质为分子晶体,
故答案为:分子晶体;
(5)价电子数相等,原子个数相等的微粒为等电子体,故与CO互为等电子体的二价阴离子为C22-,Ni(CO)4中Ni与CO的C原子形成配位键,形成四面体结构,其结构图为 ,
,
故答案为:C22-; .
.
点评 本题考查了物质结构和性质,涉及等电子体、原子的杂化方式、晶体类型的判断、核外电子排布式的书写等知识点,这些知识点都是高考热点,会根据均摊法确定物质的化学式、根据价层电子对互斥理论确定原子杂化方式及分子空间构型,难度中等.

练习册系列答案
相关题目
2.下列离子方程式与所述事实相符的是( )
| A. | Na2S2O3溶液中加入稀盐酸:2S2O32-+2H+=SO42-+3S+H2O | |
| B. | 将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO | |
| C. | 向含有0.4molFeBr2的溶液中通入0.3molCl2充分反应4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 | |
| D. | 向Al2(SO4)3溶液中加入过量氨水:Al3++4NH3•H2O=AlO2-+4NH4+ |
18.在盛有稀碳酸钠溶液的烧杯中插入惰性电极,电解一时间后,溶液中无晶体析出,则下列说法错误的是( )
| A. | 溶液的浓度增大 | |
| B. | 溶液的pH增大 | |
| C. | 溶液中钠离子与碳酸根离子的物质的量之比变小 | |
| D. | 溶液的质量分数不变 |
19.氢氧燃料电池是将H2和O2分别通入电池,穿过浸入20%-40%的KOH溶液的多孔碳电极,其电池反应为2H2+4OH--4e-═4H2O和O2+2H2O+4e-═4OH-,则下列叙述正确的( )
| A. | 通氢气的一极是正极,通氧气的一极是负极 | |
| B. | 通氢气的一极发生的是还原反应 | |
| C. | 工作一段时间后电解质溶液的pH值减小 | |
| D. | 工作时负极区附近的pH值增大 |
16.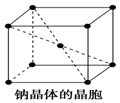 金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
 金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )| A. | $\root{3}{\frac{2a}{{N}_{A}ρ}}$ | B. | $\sqrt{2}$$\root{3}{\frac{2a}{{N}_{A}ρ}}$ | C. | $\frac{\sqrt{3}}{4}$$\root{3}{\frac{2a}{{N}_{A}ρ}}$ | D. | $\frac{1}{2}$$\root{3}{\frac{2a}{{N}_{A}ρ}}$ |
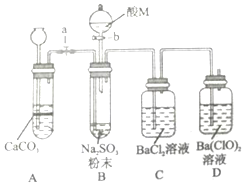 SO2是一种有毒气体,但可用于酒精的防腐剂,可以抵抗微生物的侵袭.甲同学用Na2SO4制备SO2,并验证SO2的部分性质.设计了如下实验步骤及装置:
SO2是一种有毒气体,但可用于酒精的防腐剂,可以抵抗微生物的侵袭.甲同学用Na2SO4制备SO2,并验证SO2的部分性质.设计了如下实验步骤及装置: