题目内容
如下性质的递变中,不正确的是( )
| A、HCl、H2S、PH3的稳定性依次减弱 |
| B、HClO4、H2SO4、H3PO4、H4SiO4的酸性依次减弱(相同条件下) |
| C、CsOH、KOH、LiOH的碱性依次减弱 |
| D、Na+、Mg2+、Al3+的氧化性依次减弱 |
考点:非金属在元素周期表中的位置及其性质递变的规律,金属在元素周期表中的位置及其性质递变的规律,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.非金属性越强,气态氢化物越稳定;
B.非金属性越强,最高价氧化物的水化物的酸性越强;
C.金属性越强,最高价氧化物的水化物的碱性越强;
D.金属性越强,对应离子的氧化性越弱.
B.非金属性越强,最高价氧化物的水化物的酸性越强;
C.金属性越强,最高价氧化物的水化物的碱性越强;
D.金属性越强,对应离子的氧化性越弱.
解答:
解:A.非金属性Cl>S>P,则HCl、H2S、PH3的稳定性依次减弱,故A正确;
B.非金属性Cl>S>P>Si,最高价氧化物的水化物的酸性为HClO4、H2SO4、H3PO4、H4SiO4的酸性依次减弱,故B正确;
C.金属性Cs>K>Li,最高价氧化物的水化物的碱性为CsOH、KOH、LiOH的碱性依次减弱,故C正确;
D.金属性Na>Mg>Al,则Na+、Mg2+、Al3+的氧化性依次增强,故D错误;
故选D.
B.非金属性Cl>S>P>Si,最高价氧化物的水化物的酸性为HClO4、H2SO4、H3PO4、H4SiO4的酸性依次减弱,故B正确;
C.金属性Cs>K>Li,最高价氧化物的水化物的碱性为CsOH、KOH、LiOH的碱性依次减弱,故C正确;
D.金属性Na>Mg>Al,则Na+、Mg2+、Al3+的氧化性依次增强,故D错误;
故选D.
点评:本题考查金属性、非金属性的比较,为高频考点,把握元素的位置及元素周期律为解答的关键,注意常见的金属性、非金属性比较方法及应用,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
下列说法正确的是( )
A、1mol阿司匹林(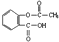 )与足量的NaOH溶液反应,消耗NaOH最大的物质的量为2mol )与足量的NaOH溶液反应,消耗NaOH最大的物质的量为2mol |
| B、汽油、柴油等矿物油与植物油主要成分都是烃,均可以萃取溴水中的溴 |
| C、丙氨酸和苯丙氨酸脱水,最多可生成4种二肽 |
D、按系统命名法,化合物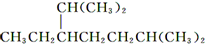 的名称为2甲基5异丙基庚烷 的名称为2甲基5异丙基庚烷 |
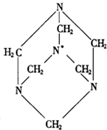 环六次甲基四胺是一种重要的化工原料,其结构式如图所示.下列关于环六次甲基四胺分子结构的叙述中正确的是( )
环六次甲基四胺是一种重要的化工原料,其结构式如图所示.下列关于环六次甲基四胺分子结构的叙述中正确的是( )| A、分子中所有的N,C原子共面 |
| B、结构式中打*的N原子处于分子的中心 |
| C、分子中含有3个相同的C,N交替排列的六元环 |
| D、连接分子中的4个N原子可构成一个正四面体 |
与NH4+具有相同电子总数和质子总数的是( )
| A、Na+ |
| B、F- |
| C、Ne |
| D、K+ |
下列物质不能使溴水褪色但能使KMnO4酸性溶液褪色的是( )
| A、乙烷 | B、丁烯 | C、苯 | D、乙苯 |
已知a元素的阳离子,b元素的阴离子、c元素的阴离子具有相同的电子层结构,且b的阴离子半径大于c的阴离子半径,则其原子序数大小顺序为( )
| A、c>b>a |
| B、a>b>c |
| C、a>c>b |
| D、c>a>b |
分析下表,下列选项中错误的是( )
| 化学式 | NH3?H2O | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7, K2=5.6×l0-11 |
| A、0.1mol?L-1 CH3COONa溶液显碱性,0.1mol?L-1 CH3COONH4溶液显中性 |
| B、等物质的量浓度的NaHCO3和NaCN溶液,前者溶液中水的电离程度大 |
| C、NaCN+H2O+CO2(少量)=HCN+NaHCO3 |
| D、上述3种等体积等pH的酸溶液,分别加水稀释后pH仍相等,则醋酸中加入水的体积最少 |
下列表示物质结构的化学用语或模型正确的是( )
A、对硝基甲苯的结构简式: |
B、CH4分子的球棍模型: |
C、醛基的电子式: |
| D、葡萄糖的最简式(实验式):CH2O |
下列说法正确的是( )
A、高聚物脲醛树脂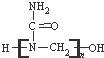 的合成单体之一是CH3OH 的合成单体之一是CH3OH |
B、按系统命名法,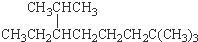 的名称为2,7,7-三甲基-3-乙基辛烷 的名称为2,7,7-三甲基-3-乙基辛烷 |
| C、有一种信息素的结构简式为CH3(CH2)5CH═CH(CH2)9CHO,为验证该物质中既含有醛基又含有碳碳双键,向该物质的试液中先加溴的CCl4溶液,观察到溶液褪色,继续滴加直到溶液变为红棕色,再向溶液中加入0.5mL H2O,充分振荡,观察到溶液褪色 |
D、化合物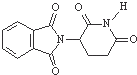 的分子式为C13H8O4N2 的分子式为C13H8O4N2 |