题目内容
2.下列叙述正确的是( )| A. | 鸡蛋白溶胶中加入饱和硫酸铵溶液后有蛋白质析出 | |
| B. | 直径介于1nm~100nm之间的微粒称为胶体 | |
| C. | 因为液态氟化氢中存在氢键,所以其分子比氯化氢更稳定 | |
| D. | 电泳现象可证明胶体属于电解质溶液 |
分析 A、鸡蛋白蛋白质,能遇铵盐溶液发生盐析;
B、分散系的本质区别是分散质直径的大小;
C、氢键只能影响到熔沸点;
D、电泳现象说明胶体中的胶粒带电.
解答 解:A、鸡蛋白蛋白质,能遇铵盐溶液发生盐析,故饱和的硫酸铵溶液能使鸡蛋白溶液中的蛋白质析出,故A正确;
B、分散系的本质区别是分散质直径的大小,其中胶体的胶粒直径介于1-100nm之间,但由于胶体是混合物,故只能说直径介于1-100nm之间的微粒形成的分散系为胶体,故B错误;
C、氢键只能影响到熔沸点,影响稳定性的是分子内的化学键,故HF的稳定性比HCl强,与HF分子间存在氢键无关,故C错误;
D、电泳现象说明胶体中的胶粒带电,但不能证明其是电解质溶液,故D错误.
故选A.
点评 本题综合考查了胶体、蛋白质的性质和氢键对物质的熔沸点的影响,应注意的是氢键是分子之间的作用力,故不影响物质的稳定性.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
12.某溶液中有:①Cu2+、②NH4+、③Fe2+、④Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再向其中加入过量盐酸,溶液中大量减少的阳离子是( )
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
13.实验室中的药品常按物质的性质、类别等有规律地摆放.现有部分药品按某种规律的摆放在实验桌上,如下图.做“硫酸的性质”的实验时,某同学取用BaCl2溶液后,应把它放回的位置是( )
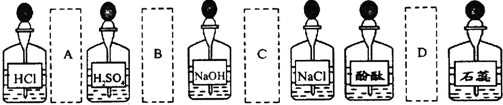

| A. | A | B. | B | C. | C | D. | D |
10.能把稀硫酸、氢氧化钠和氯化钠三种溶液一次性鉴别出来的试剂是( )
| A. | 紫色石蕊溶液 | B. | 无色酚酞溶液 | C. | 碳酸钠溶液 | D. | 硝酸钾溶液 |
17.制备硅单质时,主要化学反应如下:
(1)SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
(2)Si+2Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$SiCl4
(3)SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl
下列对上述三个反应的叙述中,不正确的是( )
(1)SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
(2)Si+2Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$SiCl4
(3)SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl
下列对上述三个反应的叙述中,不正确的是( )
| A. | (1)(3)为置换反应 | B. | (2)为化合反应 | ||
| C. | 只有(1)(3)为氧化还原反应 | D. | (1)(2)(3)均为氧化还原反应 |
7.下列数据记录合理的是( )
| A. | 用托盘天平称取8.75 g食盐 | |
| B. | 用25 mL量筒量取12.36 mL盐酸 | |
| C. | 用广泛pH试纸测得某溶液pH值为3.5 | |
| D. | 温度计上显示的室温读数为25.6℃ |
14.在从碘水中萃取碘的实验中,下列说法正确的是( )
| A. | 萃取剂要求不溶于水,且比水更容易使碘溶解 | |
| B. | 注入碘水和萃取剂,倒转分液漏斗反复用力振荡后立即分液 | |
| C. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| D. | 实验室如果没有四氯化碳,可以用酒精代替 |
11.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 16g O2和O3的混合气体中含有的原子数为NA | |
| B. | 在1L0.1 mol/L碳酸钠溶液中,CO32-总数为0.1 NA | |
| C. | 标准状况下,22.4 LSO3与水反应生成1mol硫酸 | |
| D. | 标准状况下,22.4L Cl2完全发生氧化还原反应一定转移2NA个电子 |
 ,该化合物中化学键类型有离子键、共价键.
,该化合物中化学键类型有离子键、共价键. .
.