题目内容
下列说法中正确的是( )
| A、PCl3分子结构呈三角锥形,P原子采用sp3杂化 |
| B、sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成 |
| C、凡中心原子采取sp3杂化的分子,其分子的几何构型都是四面体 |
| D、AB3型的分子空间构型必为平面三角形 |
| E、AB3型的分子空间构型必为平面三角形 |
考点:判断简单分子或离子的构型,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:A.根据价层电子对互斥理论确定分子构型,存在sp3杂化类型的原子含有4个价层电子对;
B.同一原子中,能量相近的轨道才可以杂化,杂化是指同一电子层的轨道杂化;
C.中心原子采取sp3杂化的分子,VSEPR模型是正四面体,但其立体构形不一定是正四面体;
D. AB3型的分子空间构型不一定为平面三角形;
B.同一原子中,能量相近的轨道才可以杂化,杂化是指同一电子层的轨道杂化;
C.中心原子采取sp3杂化的分子,VSEPR模型是正四面体,但其立体构形不一定是正四面体;
D. AB3型的分子空间构型不一定为平面三角形;
解答:
解:A.PCl3分子中价层电子对=3+
=4,所以采取sp3杂化,该分子中含有一个孤电子对,所以其空间构型是三角锥型,故A正确;
B.SP3杂化是指同一电子层的1个S轨道和3个P轨道杂化形成的4个SP3杂化轨道,故B错误;
C.中心原子采取sp3杂化的分子,VSEPR模型是正四面体,但其立体构形不一定是正四面体,如:水和氨气分子中中心原子采取sp3杂化,但H2O是V型,NH3是三角锥型,故C错误;
D.AB3型的分子空间构型不一定为平面三角形,价层电子对个数是3且不含孤电子对为平面三角形,如甲醛分子中碳原子含有3个σ键且不含孤电子对,所以其价层电子对个数是3,则立体构型为平面三角形;氨气分子中氮原子价层电子对个数=3+
(5-3×1)=4,且含有一个孤电子对,所以其立体构型是三角锥形,故D错误;
故选A.
| 1 |
| 2 |
B.SP3杂化是指同一电子层的1个S轨道和3个P轨道杂化形成的4个SP3杂化轨道,故B错误;
C.中心原子采取sp3杂化的分子,VSEPR模型是正四面体,但其立体构形不一定是正四面体,如:水和氨气分子中中心原子采取sp3杂化,但H2O是V型,NH3是三角锥型,故C错误;
D.AB3型的分子空间构型不一定为平面三角形,价层电子对个数是3且不含孤电子对为平面三角形,如甲醛分子中碳原子含有3个σ键且不含孤电子对,所以其价层电子对个数是3,则立体构型为平面三角形;氨气分子中氮原子价层电子对个数=3+
| 1 |
| 2 |
故选A.
点评:本题考查了粒子空间构型的判断,侧重考查了sp3杂化轨道理论,根据价层电子对互斥理论来分析解答,题目难度中等.

练习册系列答案
相关题目
下列选项中,水既不是氧化剂,又不是还原剂的是( )
| A、2F2+2H2O=4HF+O2↑ | ||||
B、2NaCl+2H2O
| ||||
| C、3NO2+H2O=2HNO3+2NO | ||||
| D、2Na+2H2O=2NaOH+H2↑ |
下列强电解质、弱电解质、非电解质的分类,正确的一组是( )
| A | B | C | D | |
| 强电解质 | CH3COOH | NaOH | BaSO4 | CuSO4 |
| 弱电解质 | Al | CH3COOH | CaCO3 | NH3?H2O |
| 非电解质 | CO2 | 金刚石 | 水银 | 酒精 |
| A、A | B、B | C、B | D、D |
下列属于吸热反应的是( )
| A、铁与稀盐酸 |
| B、氢氧化钠与硫酸的中和反应 |
| C、煅烧石灰石 |
| D、炸药爆炸 |
有一种高分子材料称为“塑料王”,它的成分是( )
| A、聚乙烯 | B、聚苯乙烯 |
| C、聚四氟乙烯 | D、聚氨酯树脂 |
在NH4Cl溶液中,下列关系正确的是( )
| A、c (Cl-)>c (NH4+)>c (H+)>c (OH-) |
| B、c (NH4+)>c (Cl-)>c (H+)>c (OH-) |
| C、c (NH4+)=c (Cl-)>c (H+)=c (OH-) |
| D、c (Cl-)=c (NH4+)>c (H+)>c (OH-) |
生活中常用的塑料及橡胶制品都属于( )
| A、传统非金属无机材料 |
| B、新型非金属无机材料 |
| C、高分子材料 |
| D、复合材料 |
 利用太阳能分解水生成的氢气,在催化剂作用下氢气与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题:
利用太阳能分解水生成的氢气,在催化剂作用下氢气与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题: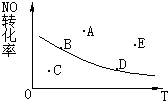 2NO+O2?2NO2+Q,NO的最大转化率与温度的关系图上标有A、B、C、D、E五点,其中表示未达到平衡状态且υ正>υ逆的是( )
2NO+O2?2NO2+Q,NO的最大转化率与温度的关系图上标有A、B、C、D、E五点,其中表示未达到平衡状态且υ正>υ逆的是( )