题目内容
标准状况下,1L水中溶解700体积的氨气,所得溶液的密度为0.9g/cm3,则氨水的浓度为 .
考点:溶液中溶质的质量分数及相关计算
专题:计算题
分析:先计算出标况下700L氨气的物质的量,再计算出氨气的质量、氨水的质量分数,最后根据c=
计算出该氨水的物质的量浓度.
| 1000ρw |
| M |
解答:
解:标况下700L氨气的物质的量为:
=
mol,氨气的质量为:17g/mol×
mol=531.25g,
1L水的质量约为1000g,则该氨水的质量分数为:
×100%≈34.7%,
该氨水的物质的量浓度为:c=
=
mol/L≈18.4mol/L,
故答案为:18.4mol/L.
| 700L |
| 22.4L/mol |
| 700 |
| 22.4 |
| 700 |
| 22.4 |
1L水的质量约为1000g,则该氨水的质量分数为:
| 531.25g |
| 1000g+531.25g |
该氨水的物质的量浓度为:c=
| 1000ρw |
| M |
| 1000×0.9×34.7% |
| 17 |
故答案为:18.4mol/L.
点评:本题考查了物质的量浓度的计算,题目难度不大,试题侧重基础知识的考查,明确物质的量浓度的概念及表达式即可解答,注意氨水的体积不是水的体积.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
下列溶液中含Cl-浓度最大的是( )
| A、10m1,0.1mol?L-1的AlC13溶液 |
| B、20m1,0.1mo1?L-1的CaC12溶液 |
| C、30m1,0.2mo1?L-1的KC1溶液 |
| D、100m1,0.25mo1?L-1的NaC1溶液 |
下列化学用语表达正确的是( )
A、碳-12原子
| ||
B、N2电子式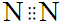 | ||
| C、次氯酸的结构式 H-Cl-O | ||
D、硫离子结构示意图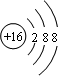 |
实验室需配制 100mL 1.5mol/L NaOH 溶液,下列叙述正确的是( )
| A、转移液体时,玻璃棒应紧靠容量瓶口 |
| B、容量瓶上标有温度、浓度、容积和压强 |
| C、将所需的6.0g氢氧化钠固体倒入到容量瓶中溶解 |
| D、定容时若俯视刻度线观察液面,会使所配制的NaOH 溶液的浓度偏高 |


