题目内容
16.金属钠的化学性质非常活泼.(1)钠与冷水剧烈反应,写出钠与水反应的化学方程式2Na+2H2O=H2↑+2NaOH.
(2)将钠投入氯化铁溶液中,观察到的现象是有大量气泡生成,有红褐色沉淀生成.
(3)钠在空气中燃烧生成Na2O2,写出Na2O2的电子式
 .
.(4)Na2O2可作供氧剂,写出Na2O2与CO2反应的化学方程式2Na2O2+2CO2═2Na2CO3+O2.
当有0.2mol电子发生转移时,生成氧气的体积为2.24LL(标准状态).
分析 (1)钠和水反应生成氢氧化钠和氢气;
(2)钠投入到氯化铁溶液中:钠和水反应生成氢氧化钠和氢气,溶液呈碱性,氢氧化钠和氯化铁反应生成红褐色沉淀氢氧化铁;
(3)Na2O2是离子化合物,由Na+离子和O2-离子构成,Na2O2的电子式为 ;
;
(4)Na2O2与CO2反应生成碳酸钠和氧气.
解答 解:(1)钠和水反应生成氢氧化钠和氢气,反应方程式为:2Na+2H2O=H2↑+2NaOH,故答案为:2Na+2H2O=H2↑+2NaOH;
(2)钠投入到FeCl3溶液中,发生反应为:2Na+2H2O═2NaOH+H2↑,3NaOH+FeCl3═Fe(OH)3↓+3NaCl,既有Na与H2O反应现象,又有NaOH与FeCl3反应现象.所以现象为:钠浮在液面上,与溶液剧烈反应,熔成小球,四处游动,发出嘶嘶声,有气泡冒出,有红褐色沉淀生成;故答案为:有大量气泡生成,有红褐色沉淀生成;(3)Na2O2是离子化合物,由Na+离子和O2-离子构成,Na2O2的电子式为 ,故答案为:
,故答案为: ;
;
(4)Na2O2与CO2反应生成碳酸钠和氧气,该反应为2Na2O2+2CO2═2Na2CO3+O2,当有0.2mol电子发生转移时,生成0.1mol的氧气,所以氧气的体积为2.24L,
故答案为:2Na2O2+2CO2═2Na2CO3+O2;2.24L.
点评 本题考查化学反应方程式的书写,明确物质的性质及发生的化学反应是解答的关键,难度不大,学生应熟练掌握化学用语的使用.

练习册系列答案
相关题目
6.1摩某有机物在稀硫酸作用下,水解生成2摩相同的物质.下列物质中:
①蔗糖 ②麦芽糖 ③淀粉④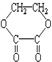 ⑤
⑤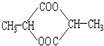 ⑥
⑥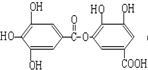 ⑦
⑦
符合题意的物质可能是( )
①蔗糖 ②麦芽糖 ③淀粉④
 ⑤
⑤ ⑥
⑥ ⑦
⑦
符合题意的物质可能是( )
| A. | ②⑤⑥⑦ | B. | ②④⑤⑦ | C. | ①②⑤⑦ | D. | ①④⑤⑥ |
7.元素周期表和元素周期律可以指导人们进行规律性的推测和判断.下列说法不合理的是( )
| A. | 若X+和Y2-的核外电子层结构相同,则原子序数:X>Y | |
| B. | 元素周期表中位于金属和非金属分界线附近能找到半导体的元素 | |
| C. | Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH>Ba(OH)2 | |
| D. | 由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
11.合理饮食是保证我们身体健康的前提,下列关于饮食的说法正确的是( )
| A. | 水果、蔬菜含有丰富的维生素,若要减肥,每天只吃水果蔬菜即可 | |
| B. | 米饭含有大量的淀粉,成人每天食用量不能超过100g | |
| C. | 要促进身体健康,各种饮食必须合理搭配 | |
| D. | 鸡蛋含丰富的蛋白质,人体所需蛋白质都可由鸡蛋提供,多吃有益 |
1.下列说法正确的是( )
| A. | 石油分馏的各馏分均是纯净物 | |
| B. | 乙烯和苯都能使酸性KMnO4溶液褪色 | |
| C. | 淀粉和纤维素水解的最终产物都是葡萄糖 | |
| D. | 溴乙烷与NaOH水溶液共热生成乙烯 |
5.按碳骨架分类,下列说法正确的是( )
| A. | CH3CH(CH3)2属于链状化合物 | B. |  属于芳香族化合物 属于芳香族化合物 | ||
| C. | 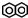 属于脂环化合物 属于脂环化合物 | D. | 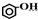 属于芳香化合物 属于芳香化合物 |
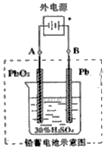 铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题:
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题: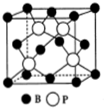 氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.