题目内容
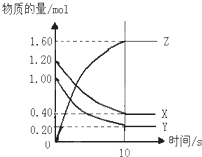 如右图所示,某温度下,物质的量分别是1.2mol的气体X和物质的量为1.0mol的气体Y,在2L密闭容器中反应生成气体Z,反应5min后测得n(X)=0.4mol,n(Y)=0.2mol,生成的n(Z)=1.6mol,则该反应的化学方程式可表示为
如右图所示,某温度下,物质的量分别是1.2mol的气体X和物质的量为1.0mol的气体Y,在2L密闭容器中反应生成气体Z,反应5min后测得n(X)=0.4mol,n(Y)=0.2mol,生成的n(Z)=1.6mol,则该反应的化学方程式可表示为考点:化学平衡建立的过程,反应速率的定量表示方法
专题:化学平衡专题
分析:根据图象分析可知,随反应进行反应物减小,生成物增大,反应开始达到化学平衡状态,依据消耗X、Y、Z物质的量之比等于化学方程式系数之比计算得到化学方程式,根据v=
求出v(Z).
| △c |
| △t |
解答:
解:根据图象分析可知,随反应进行反应物X、Y物质的量减小,生成物Z的物质的量增大,反应开始达到化学平衡状态,所以X、Y是反应物,Z是产物,消耗X、Y、Z物质的量之比等于化学方程式系数之比,即为(1.2-0.4):(1.0-0.2):(1.6-0)=0.8:0.8:1.6=1:1:2,方程式为:X+Y?2Z,反应在10分钟内的化学反应速率用Z来表示则V(Z)=
=0.08mol/(L?min),
故答案为:X+Y?2Z;0.08mol/(L?min).
| ||
| 10mn |
故答案为:X+Y?2Z;0.08mol/(L?min).
点评:本题考查了化学平衡的有关计算,难度不大,该反应的速率可以用定义法也可以用化学计量法,图象分析,化学方程式书写方法是关键,题目难度中等.

练习册系列答案
相关题目
氯气与碘在加热的条件下以一定比例反应可得的一红棕色液体ICl(氯化碘),ICl的性质类似于卤素,有很强的化学活动性.例如:ICl+H2O═HCl+HIO,2Zn+2ICl═ZnCl2+ZnI2,下列叙述正确的是( )
| A、在Zn跟ICl的反应中,ZnI2既是氧化产物又是还原产物 |
| B、在H2O跟ICl的反应中,ICl是氧化剂H2O是还原剂 |
| C、在Zn跟ICl的反应中,ZnCl2既是氧化产物又是还原产物 |
| D、在H2O跟ICl的反应中,ICl既是氧化剂又是还原剂 |
下列各物质中所含的少量杂质,用括号内的物质能除去,并且不引进其他杂质的是 ( )
| A、二氧化碳中所含的氯化氢(NaOH溶液) |
| B、氢气中所含的硫化氢(硫酸铜溶液) |
| C、乙酸乙酯中所含的乙酸(乙醇) |
| D、氯化钠溶液中所含的氯化钡(硫酸) |
配制0.1mol/L碳酸钠溶液100mL,不需要用到的仪器是( )
| A、100 mL量筒 |
| B、电子天平 |
| C、100 mL容量瓶 |
| D、胶头滴管 |
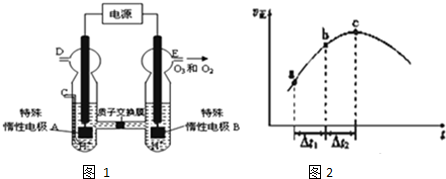
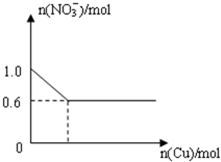 将28.8g铜投入100mL浓硝酸中,最后铜有剩余,其NO3-离子物质的量变化如图所示,请回答下列问题:
将28.8g铜投入100mL浓硝酸中,最后铜有剩余,其NO3-离子物质的量变化如图所示,请回答下列问题: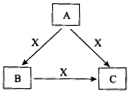 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.若A、B、C的焰色反应均呈黄色,水溶液均为碱性.
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.若A、B、C的焰色反应均呈黄色,水溶液均为碱性.