题目内容
10.(1)常温下,0.1mol/L的甲酸和0.1mol/L的盐酸各100mL,分别与足量的同浓度氢氧化钾溶液反应所需氢氧化钾溶液的体积前者=后者(选填“>”、“<”或“=”).(2)常温下,0.1mol/L的甲酸和pH=1的甲酸各100mL,分别与足量的碳酸氢钠溶液反应,产生的气体前者比后者少(选填“多”、“少”或“=”).
(3)在25℃条件下,将pH=10的偏铝酸钠溶液稀释100倍,稀释后溶液的pH为(填选项字母,下同)D.
A.10 B.8
C.10~12之间 D.8~10之间
(4)25℃时,向0.1mol/L的甲酸溶液中加入少量甲酸钠晶体,当晶体溶解后测得溶液pH将A.
A.增大 B.减小
C.不变 D.无法确定
(5)室温下,向0.1mol/L的H2SO4中加入足量的锌粒,若想减慢H2产生的速率,但又不影响H2的体积,可以向硫酸溶液中加入BD试剂.
A.硫化钠晶体 B.甲酸钠晶体
C.少量银粉 D.硫酸钠溶液.
分析 (1)甲酸和盐酸都是一元酸,盐酸和甲酸与KOH完全中和时消耗KOH的物质的量与酸的物质的量成正比;
(2)甲酸是弱酸,在水溶液中部分电离,所以pH=1的甲酸其物质的量浓度大于0.1mol/L,0.1mol/L、pH=1的两种甲酸溶液分别与足量碳酸氢钠反应,生成二氧化碳的物质的量与甲酸的物质的量成正比;
(3)偏铝酸钠是强碱弱酸盐,加水稀释促进其水解,但其水解增大程度小于溶液体积增大程度,所以稀释后溶液pH减小,但溶液中c(OH-)大于原来的$\frac{1}{100}$;
(4)甲酸钠在水溶液中电离导致溶液中甲酸根离子浓度增大,所以抑制甲酸电离,溶液中c(H+)降低;
(5)减慢H2产生的速率,但又不影响H2的体积,说明改变条件时能降低氢离子浓度,但电离出的氢离子总物质的量不变.
解答 解:(1)甲酸和盐酸都是一元酸,盐酸和甲酸与KOH完全中和时消耗KOH的物质的量与酸的物质的量成正比,甲酸和盐酸的体积及浓度都相等,则其物质的量相等,所以消耗等浓度的KOH溶液体积相等,故答案为:=;
(2)甲酸是弱酸,在水溶液中部分电离,所以pH=1的甲酸其物质的量浓度大于0.1mol/L,0.1mol/L、pH=1的两种甲酸溶液分别与足量碳酸氢钠反应,生成二氧化碳的物质的量与甲酸的物质的量成正比,前者的甲酸物质的量小于后者,则生成的二氧化碳前者比后者少,故答案为:少;
(3)偏铝酸钠是强碱弱酸盐,加水稀释促进其水解,但其水解增大程度小于溶液体积增大程度,所以稀释后溶液pH减小,但溶液中c(OH-)大于原来的$\frac{1}{100}$,所以溶液的pH在8-10之间,故选D;
(4)甲酸钠在水溶液中电离导致溶液中甲酸根离子浓度增大,所以抑制甲酸电离,溶液中c(H+)降低,则溶液的pH增大,故选A;
(5)减慢H2产生的速率,但又不影响H2的体积,说明改变条件时能降低氢离子浓度,但电离出的氢离子总物质的量不变,
A.硫化钠晶体和稀硫酸反应生成硫化氢,导致生成的氢气减少,故A不选;
B.甲酸钠晶体和稀硫酸反应生成甲酸,甲酸是弱电解质,溶液中氢离子浓度降低,但电离出总氢离子物质的量不变,所以反应速率降低但生成氢气体积不变,故B选;
C.加入少量银粉,Ag、Zn和稀硫酸构成原电池,加快反应速率,故C不选;
D.加入硫酸钠溶液,溶液中氢离子浓度降低,但电离出总氢离子物质的量不变,所以能降低反应速率但生成氢气总量不变,故D选;
故选BD.
点评 本题考查酸碱混合溶液定性判断及弱电解质的电离,为高频考点,明确弱电解质电离特点、酸碱中和反应实质是解本题关键,注意(5)中C选项加快反应速率,题目难度不大.

| A. | 用分液漏斗分离除去溴苯中混入的溴 | |
| B. | 用渗析法除去Fe(OH)3胶体中的Cl- | |
| C. | 除去溴乙烷中的乙醇,用水洗后,再用分液漏斗分离 | |
| D. | 用盐析法分离硬脂酸钠和甘油 |
| A. | 在一个基态多电子的原子中,不可能有两个能量完全相同的电子 | |
| B. | M层全充满而N层为4s2的原子与核外电子排布式为1s22s22p63s23p63d64s2的原子位于同一族 | |
| C. | 如果某一基态原子3p能级上仅有2个电子,它们的自旋状态必然相同 | |
| D. | 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
| A. | Na+、HCO3-、K+、OH- | B. | Fe2+、H+、SO42-、NO3- | ||
| C. | Fe3+、SCN-、NH4+、Cl- | D. | AlO2-、OH-、Na+、NH4+ |
①卤素的钾盐中,所有卤素的化合价均为-1价
②溴中溶有少量氯气,可以用加入溴化钠再用苯萃取的方法提纯
③溴化银具有感光性,碘化银不具有感光性
④某溶液与淀粉KI溶液混合后出现蓝色,则证明该溶液是氯水或溴水
⑤氯气与水溶液反应,一定有酸生成⑥氯气跟水反应时,水既不作氧化剂也不是还原剂.
| A. | ①③⑤ | B. | ②③⑥ | C. | ②⑤⑥ | D. | ①③④ |
| A. | H2与Cl2混合后点燃与 H2 在Cl2中安静燃烧的反应速率是一样大的 | |
| B. | 反应物所具有的总能量高于产物所具有的总能量 | |
| C. | 断开1mol H-H键和1mol Cl-Cl键所吸收的总能量小于形成1mol H-Cl键所放出的能量 | |
| D. | 该反应中,化学能只转变为热能 |
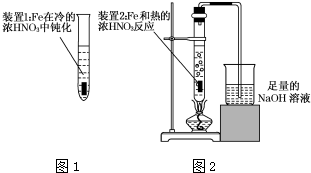 Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题:
Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质.请你参与研究并回答下列问题: 随着对合成氨研究的发展,希腊科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图).钯电极A是电解池的阴极(填“阳”或“阴”),该极上的电极反应式是N2+6e-+6H+═2NH3.
随着对合成氨研究的发展,希腊科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图).钯电极A是电解池的阴极(填“阳”或“阴”),该极上的电极反应式是N2+6e-+6H+═2NH3.