题目内容
在实验室中,氮氧化物废气(主要成分NO2和NO)可以用NaOH溶液来吸收,除去这些废气,其主要反应为:
2NO2+2NaOH→NaNO2+NaNO3+H2O NO+NO2+2NaOH→2NaNO2+H2O.(回答下列问题题)
(1)NO和NO2的混合气体的组成可表示为NOX ,该混合气体通入NaOH溶液被完全吸收时,x的值可以为 (填编号).a.1.1 b.1.2 c.1.5 d.1.8
(2)若用纯碱溶液处理氮氧化物废气,反应与上述类似,同时放出CO2.2molNO和2.4molNO2混合气体通入NaOH溶液被完全吸收时,生成的NaNO2 是 mol;生成的NaNO3是 mol.
(3)若在标准状况下,2.016 L氮氧化物的混合气和0.896LO2与1mol/LNa2CO3溶液50mL恰好反应生成NaNO3,则混和气体中N2O4与NO2的体积比为 .
(4)现有标准状况下a升NO2(其中N2O4体积分数为20%)和b升NO的混合气恰好被200mL Na2CO3溶液完全吸收,则a、b应满足的关系为: ;该Na2CO3溶液的物质的量浓度为 mol/L(用含a、b的代数式表示).请写出纯碱溶液吸收NO2的化学方程式: .
2NO2+2NaOH→NaNO2+NaNO3+H2O NO+NO2+2NaOH→2NaNO2+H2O.(回答下列问题题)
(1)NO和NO2的混合气体的组成可表示为NOX ,该混合气体通入NaOH溶液被完全吸收时,x的值可以为
(2)若用纯碱溶液处理氮氧化物废气,反应与上述类似,同时放出CO2.2molNO和2.4molNO2混合气体通入NaOH溶液被完全吸收时,生成的NaNO2 是
(3)若在标准状况下,2.016 L氮氧化物的混合气和0.896LO2与1mol/LNa2CO3溶液50mL恰好反应生成NaNO3,则混和气体中N2O4与NO2的体积比为
(4)现有标准状况下a升NO2(其中N2O4体积分数为20%)和b升NO的混合气恰好被200mL Na2CO3溶液完全吸收,则a、b应满足的关系为:
考点:化学方程式的有关计算,氮的氧化物的性质及其对环境的影响,有关混合物反应的计算
专题:计算题
分析:(1)由方程式2NO2+2NaOH=NaNO2+NaNO3+H2O和NO+NO2+2NaOH=2NaNO2+H2O可知,NO单独不能被吸收,NO和NO2混合气体被NaOH溶液被完全吸收,满足n(NO2):n(NO)≥1,当n(NO2):n(NO)=1时x值最小,计算x的最小值,因为混有NO,所以x最大值<2,据此确定x取值范围;
(2)2molNO和2.4molNO2混合气体通入NaOH溶液被完全吸收,生成物为NaNO2和NaNO3,根据反应的方程式计算;
(3)设2.016 L氮氧化物中含N2O4 x mol、NO2 y mol、NO z mol,分别利用气体总物质的量、电子守恒、钠离子及氮原子守恒列式求解;
(4)发生反应2NO2+Na2CO3=NaNO2+NaNO3+CO2 ,NO2+NO+Na2CO3=2NaNO2+CO2,从反应式就可以看出当n(NO2)/n(NO)≥1,把N2O4折换成NO2,计算a、b的关系;
恰好反应溶液溶质为NaNO2、NaNO3,由N元素守恒可知n(NaNO2)+n(NaNO3)=n(NO2)+2n(N2O4)+n(NO),由Na元素可知2n(Na2CO3)=n(NaNO2)+n(NaNO3),计算n(Na2CO3)代入c=
计算碳酸钠的浓度;
反应与NO2和NaOH反应相似,二氧化氮与碳酸钠反应生成NaNO2、NaNO3、CO2.
(2)2molNO和2.4molNO2混合气体通入NaOH溶液被完全吸收,生成物为NaNO2和NaNO3,根据反应的方程式计算;
(3)设2.016 L氮氧化物中含N2O4 x mol、NO2 y mol、NO z mol,分别利用气体总物质的量、电子守恒、钠离子及氮原子守恒列式求解;
(4)发生反应2NO2+Na2CO3=NaNO2+NaNO3+CO2 ,NO2+NO+Na2CO3=2NaNO2+CO2,从反应式就可以看出当n(NO2)/n(NO)≥1,把N2O4折换成NO2,计算a、b的关系;
恰好反应溶液溶质为NaNO2、NaNO3,由N元素守恒可知n(NaNO2)+n(NaNO3)=n(NO2)+2n(N2O4)+n(NO),由Na元素可知2n(Na2CO3)=n(NaNO2)+n(NaNO3),计算n(Na2CO3)代入c=
| n |
| V |
反应与NO2和NaOH反应相似,二氧化氮与碳酸钠反应生成NaNO2、NaNO3、CO2.
解答:
解:(1)由方程式可知,NO单独不能被吸收,NO和NO2混合气体被NaOH溶液被完全吸收,满足n(NO2):n(NO)≥1,当n(NO2):n(NO)=1时x值最小,x最小值为
=1.5,因为混有NO,所以x最大值<2,故x的取值范围为1.5≤x<2,故选:cd;
(2)2molNO和2.4molNO2混合气体通入NaOH溶液被完全吸收,
NO+NO2+2NaOH=2NaNO2+H2O
1mol 1mol 2mol
2mol 2mol 4mol
反应后剩余0.4molNO2,
2NO2+2NaOH=NaNO2+NaNO3+H2O
2mol 1mol 1mol
0.4mol 0.2mol 0.2mol
则生成的NaNO2的物质的量为4mol+0.2mol=4.2mol、NaNO3物质的量为0.2mol,
故答案为:4.2mol;0.2mol;
(3)设2.016 L氮氧化物中含N2O4 x mol、NO2 y mol、NO z mol,
x+y+z=
=0.09
2x+y+3z=
×4 (得失电子守恒)
2 x+y+z=0.05×2 (氮原子子守恒、钠离子守恒)
解得:x=0.01(mol),y=0.05(mol),z=0.03(mol)
∴V(N2O4):V(NO2)=n(N2O4):n(NO2)=0.01:0.05=1:5,
故答案为:1:5;
(4)发生反应2NO2+Na2CO3=NaNO2+NaNO3+CO2 ,NO2+NO+Na2CO3=2NaNO2+CO2,从反应式就可以看出当n(NO2)/n(NO)≥1,气体就全部反应了,aLNO2,其中N2O4的体积分数是20%,把N2O4折换成NO2,NO2的体积总共为aL×(1-20%)+aL×20%×2=1.2aL,所以
≥1,即
≥
;
由Na元素可知2n(Na2CO3)=n(NaNO2)+n(NaNO3),由N元素守恒可知n(NaNO2)+n(NaNO3)=n(NO2)+2n(N2O4)+n(NO)=
+
+
=
mol,所以2n(Na2CO3)=
mol,故n(Na2CO3)
mol,该Na2CO3溶液的物质的量浓度为
=
mol/L,
二氧化氮与碳酸钠反应生成NaNO2、NaNO3、CO2,反应方程式为2NO2+Na2CO3=NaNO2+NaNO3+CO2 ,
故答案为:
≥
;
;2NO2+Na2CO3=NaNO2+NaNO3+CO2 .
| 2+1 |
| 2 |
(2)2molNO和2.4molNO2混合气体通入NaOH溶液被完全吸收,
NO+NO2+2NaOH=2NaNO2+H2O
1mol 1mol 2mol
2mol 2mol 4mol
反应后剩余0.4molNO2,
2NO2+2NaOH=NaNO2+NaNO3+H2O
2mol 1mol 1mol
0.4mol 0.2mol 0.2mol
则生成的NaNO2的物质的量为4mol+0.2mol=4.2mol、NaNO3物质的量为0.2mol,
故答案为:4.2mol;0.2mol;
(3)设2.016 L氮氧化物中含N2O4 x mol、NO2 y mol、NO z mol,
x+y+z=
| 2.016 |
| 22.4 |
2x+y+3z=
| 0.896 |
| 22.4 |
2 x+y+z=0.05×2 (氮原子子守恒、钠离子守恒)
解得:x=0.01(mol),y=0.05(mol),z=0.03(mol)
∴V(N2O4):V(NO2)=n(N2O4):n(NO2)=0.01:0.05=1:5,
故答案为:1:5;
(4)发生反应2NO2+Na2CO3=NaNO2+NaNO3+CO2 ,NO2+NO+Na2CO3=2NaNO2+CO2,从反应式就可以看出当n(NO2)/n(NO)≥1,气体就全部反应了,aLNO2,其中N2O4的体积分数是20%,把N2O4折换成NO2,NO2的体积总共为aL×(1-20%)+aL×20%×2=1.2aL,所以
| 1.2aL |
| bL |
| a |
| b |
| 5 |
| 6 |
由Na元素可知2n(Na2CO3)=n(NaNO2)+n(NaNO3),由N元素守恒可知n(NaNO2)+n(NaNO3)=n(NO2)+2n(N2O4)+n(NO)=
| aL(1-20%) |
| 22.4L/mol |
| aL×20%×2 |
| 22.4L/mol |
| bL |
| 22.4L/mol |
| 1.2a+b |
| 22.4 |
| 1.2a+b |
| 22.4 |
| 1.2a+b |
| 44.8 |
| ||
| 0.2L |
| 1.2a+b |
| 8.96 |
二氧化氮与碳酸钠反应生成NaNO2、NaNO3、CO2,反应方程式为2NO2+Na2CO3=NaNO2+NaNO3+CO2 ,
故答案为:
| a |
| b |
| 5 |
| 6 |
| 1.2a+b |
| 8.96 |
点评:本题考查阅读获取信息的能力、混合反应的计算等,难度中等,需要学生具备扎实的基础与利用信息、基础知识分析解决问题的能力,发现化学方程式中隐含的关系和规律是解题关键,难度较大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
下列实验装置或操作能达到实验目的是( )
A、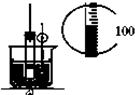 实验室制硝基苯 |
B、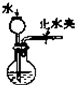 检查装置气密性 |
C、 利用排空气法收集丙烷 |
D、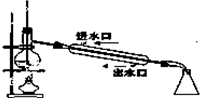 石油分馏 |
“钴酞菁(分子直径1.3×10-9m)”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似,我国科学家在世界上第一次为“钴酞菁”分子恢复了磁性.下列关于“钴酞菁”的说法正确的是( )
| A、在水中形成的分散系属于悬浊液 |
| B、分子直径比Na+小 |
| C、“钴酞菁”分子不能透过滤纸 |
| D、在水中形成的分散系具有丁达尔效应 |
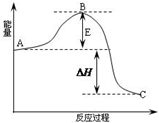 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.请回答下列问题: