题目内容
甲、乙、丙、丁、戊五种溶液的溶质分别是HCl、CH3COOH、NaOH、NH3?H2O、Na2CO3中的一种. 常温下如下实验:
①将0.1L pH=9的甲溶液分别与a L 0.001mol/L的乙溶液、b L 0.001mol/L的丁溶液充分反应后溶液呈中性时,a>b;
②浓度均为0.1mol/L的丙和丁溶液等体积混合后,溶液呈酸性;
③0.1mol/L的甲溶液pH小于0.1mol/L的戊溶液pH.
下列判断正确的是( )
①将0.1L pH=9的甲溶液分别与a L 0.001mol/L的乙溶液、b L 0.001mol/L的丁溶液充分反应后溶液呈中性时,a>b;
②浓度均为0.1mol/L的丙和丁溶液等体积混合后,溶液呈酸性;
③0.1mol/L的甲溶液pH小于0.1mol/L的戊溶液pH.
下列判断正确的是( )
| A.甲的溶质是NH3?H2O | B.乙的溶质是CH3COOH |
| C.丙的溶质是NaOH | D.戊的溶质是HCl |
由①得出以下结论:甲溶液pH=9说明甲为碱性物质,则乙、丁为HCl和CH3COOH;
中和同样的碱性物质,同浓度时乙的用量大说明乙是弱酸即为CH3COOH;则丁为HCl;由②得出以下结论:由上已知丁为HCl,浓度均为0.1 mol/L的丙和丁溶液等体积混合后,溶液呈酸性.
说明丙是弱碱即为NH3?H2O;由③得出以下结论:由上已知甲,戊分别是NaOH或Na2CO3.0.1 mol/L的甲溶液pH小于0.1 mol/L的戊溶液pH说明戊是强碱NaOH;甲是Na2CO3;
所以:甲是Na2CO3;乙是CH3COOH;丙是NH3?H2O;丁为HCl;戊是NaOH,
故选B.
中和同样的碱性物质,同浓度时乙的用量大说明乙是弱酸即为CH3COOH;则丁为HCl;由②得出以下结论:由上已知丁为HCl,浓度均为0.1 mol/L的丙和丁溶液等体积混合后,溶液呈酸性.
说明丙是弱碱即为NH3?H2O;由③得出以下结论:由上已知甲,戊分别是NaOH或Na2CO3.0.1 mol/L的甲溶液pH小于0.1 mol/L的戊溶液pH说明戊是强碱NaOH;甲是Na2CO3;
所以:甲是Na2CO3;乙是CH3COOH;丙是NH3?H2O;丁为HCl;戊是NaOH,
故选B.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
甲、乙、丙、丁、戊五种短周期元素在元素周期表中的位置如图,其中戊是金属元素.下列判断正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A、戊是两性元素 |
| B、五种元素中的金属元素中,丙的金属性最强 |
| C、简单离子半径:丙<丁 |
| D、甲的单质的熔点比丙单质的低 |


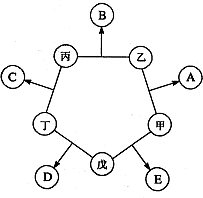 甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图所示:又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是日常生活中一种常见的金属.
甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图所示:又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是日常生活中一种常见的金属.