题目内容
14.下列各组是由等物质的量两种物质组成的混合物,投到足量的水中,充分搅拌后,不能完全溶解得到一澄清溶液的是( )| A. | 钠铝合金 | B. | Na2O和Al2O3 | C. | 明矾和BaO | D. | MgO和SO3 |
分析 设物质的量均为1mol,
A.1molNa与水反应生成1molNaOH,与等量的Al发生氧化还原反应生成偏铝酸钠和氢气;
B.1molNa2O与水反应生成2molNaOH,与1molAl2O3反应生成偏铝酸钠和水;
C.1molBaO与水反应生成1molBa(OH)2,与1mol明矾反应,碱不足,生成硫酸钡、氢氧化铝;
D.1molSO3与水反应生成1molH2SO4,与1molMgO反应生成硫酸镁和水.
解答 解:设物质的量均为1mol,
A.1molNa与水反应生成1molNaOH,与等量的Al发生氧化还原反应生成偏铝酸钠和氢气,则溶液为澄清溶液,故A不选;
B.1molNa2O与水反应生成2molNaOH,与1molAl2O3反应生成偏铝酸钠和水,则溶液为澄清溶液,故B不选;
C.1molBaO与水反应生成1molBa(OH)2,与1mol明矾反应,碱不足,生成硫酸钡沉淀、氢氧化铝沉淀,溶液变浑浊,故C选;
D.1molSO3与水反应生成1molH2SO4,与1molMgO反应生成硫酸镁和水,则溶液为澄清溶液,故D不选;
故选C.
点评 本题考查物质的性质及反应,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意过量判断及物质的量关系,题目难度不大.

练习册系列答案
相关题目
4.放热反应:3A(g)+2B(g)?4C(g),下列反应条件有利用于生成C的是( )
| A. | 低温、低压 | B. | 低温、高压 | C. | 高温、高压 | D. | 高温、低压 |
5.在一定条件下的可逆反应中,关于反应速率和达到化学平衡时,下列说法不正确的是( )
| A. | 温度只能改变某一个方向的反应速率 | |
| B. | 决定反应速率的主要因素是反应物的性质 | |
| C. | 反应体系中混合物的组成保持不变 | |
| D. | 正、逆反应速率相等但不为零 |
2.在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A. | Na+ K+ CO32- Cl- | B. | Na+ Cu2+ SO42- NO3- | ||
| C. | K+ Na+ SO42- Cl- | D. | Ba2+ HCO3- NO3- K+ |
19.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,11.2L氮气所含的原子数为NA | |
| B. | 1mol硫与铁充分反应转移的电子数为2NA | |
| C. | 常温常压下,48gSO3含有的分子数为3NA | |
| D. | 常温常压下,1molNO2气体与水反应生成NA个NO3-离子 |
6.下列基团:-CH3、-OH、-COOH、-C6H5,相互两两组成的有机物有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
3.工业制硫酸的一步重要反应是SO2在400~600℃下的催化氧化:2SO2+O2?2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下列有关说法错误的是( )
| A. | 在上述条件下,SO2不可能100%地转化为SO3 | |
| B. | 达到平衡时,SO2的浓度与SO3的浓度相等 | |
| C. | 为了提高SO2的转化率,应适当提高O2的浓度 | |
| D. | 使用催化剂是为了加快反应速率,提高生产效率 |
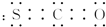 ,其分子呈直线形.
,其分子呈直线形. .
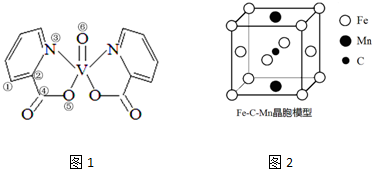
.
 根据要求回答下列有关问题:
根据要求回答下列有关问题: