题目内容
能说明0.1mol?L-1的NaHA溶液一定呈酸性的是( )
| A、某温度下,测得溶液的pH<7 |
| B、溶液中c(Na+)=c(A2-) |
| C、溶液中存在Na+、HA-、A2-、H2A 多种微粒 |
| D、NaHA溶液可与等体积等物质的量浓度的NaOH溶液恰好反应 |
考点:探究溶液的酸碱性
专题:
分析:A.温度未知,则pH<7的溶液不一定呈酸性;
B.溶液中存在电荷守恒c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),如果存在c(Na+)=c(A2-),则存在c(H+)=c(A2-)+c(HA-)+c(OH-);
C.无论溶液呈酸性还是呈碱性,都存在Na+、HA-、A2-、H2A 多种微粒;
D.NaHA溶液可与等体积等物质的量浓度的NaOH溶液恰好反应,说明NaHA是酸式盐,不能说明溶液呈酸性.
B.溶液中存在电荷守恒c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),如果存在c(Na+)=c(A2-),则存在c(H+)=c(A2-)+c(HA-)+c(OH-);
C.无论溶液呈酸性还是呈碱性,都存在Na+、HA-、A2-、H2A 多种微粒;
D.NaHA溶液可与等体积等物质的量浓度的NaOH溶液恰好反应,说明NaHA是酸式盐,不能说明溶液呈酸性.
解答:
解:A.温度未知,则pH<7的溶液不一定呈酸性,可能呈碱性,这由HA-水解和电离的相对大小判断,故A错误;
B.溶液中存在电荷守恒c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),如果存在c(Na+)=c(A2-),则存在c(H+)=c(A2-)+c(HA-)+c(OH-),则c(H+)>c(OH-),溶液呈酸性,故B正确;
C无论溶液呈酸性还是呈碱性,都存在Na+、HA-、A2-、H2A 多种微粒,所以不能据此判断该溶液呈酸性,故C错误;
D.NaHA溶液可与等体积等物质的量浓度的NaOH溶液恰好反应,说明NaHA是酸式盐,不能说明HA-水解小于电离
程度,所以不能确定该溶液呈酸性,故D错误;
故选B.
B.溶液中存在电荷守恒c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-),如果存在c(Na+)=c(A2-),则存在c(H+)=c(A2-)+c(HA-)+c(OH-),则c(H+)>c(OH-),溶液呈酸性,故B正确;
C无论溶液呈酸性还是呈碱性,都存在Na+、HA-、A2-、H2A 多种微粒,所以不能据此判断该溶液呈酸性,故C错误;
D.NaHA溶液可与等体积等物质的量浓度的NaOH溶液恰好反应,说明NaHA是酸式盐,不能说明HA-水解小于电离
程度,所以不能确定该溶液呈酸性,故D错误;
故选B.
点评:本题考查溶液酸碱性判断,根据溶液中c(H+)、c(OH-)相对大小判断溶液酸碱性,不能根据溶液pH判断溶液酸碱性,易错选项是A.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
下列分离提纯的方法正确的是( )
| A、除去氯化铵中的碘,用升华的方法 |
| B、用酒精提取碘水中的碘 |
| C、分馏法分离乙醇和乙酸 |
| D、用重结晶法除去硝酸钾中的氯化钠 |
25℃时,浓度为0.2mol?L-1的Na2CO3溶液中,下列判断不正确的是( )
| A、加热,c(OH-)增大 |
| B、存在七种粒子 |
| C、存在水解平衡,不存在电离平衡 |
| D、加热NaOH固体,恢复到原温度,C(CO32-)增大 |
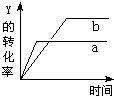 反应 X(气)+Y(气)?2Z(气)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )
反应 X(气)+Y(气)?2Z(气)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )| A、加入催化剂 | B、降低温度 |
| C、增大压强 | D、增大Y的浓度 |
某溶液中存在大量的K+、OH-、CO32-,该溶液中还可能大量存在的是( )
| A、NH4+ |
| B、Ca2+ |
| C、HCO3- |
| D、SO42- |