题目内容
有Na2SO4、Fe2(SO4)3和NaNO3的混合溶液,已知其中Fe3+的物质的量浓度为0.4mol/L,SO42-的物质的量浓度为0.7mol/L,NO3-的物质的量浓度为0.2mol/L,则此溶液中Na+的物质的量浓度为(不考虑Fe3+在溶液中的反应)( )
| A、0.2mol/L |
| B、0.3mol/L |
| C、0.4mol/L |
| D、0.35mol/L |
考点:物质的量浓度的相关计算
专题:
分析:Na2SO4、Fe2(SO4)3和NaNO3的混合溶液中一定满足电荷守恒,即:3c(Fe3+)+c(Na+)=2c(SO42-)+c(NO3-),根据铁离子、硫酸根离子、NO3-的浓度及电荷守恒计算出此溶液中Na+的物质的量浓度.
解答:
解:Na2SO4和Fe2(SO4)3的混合溶液,含Fe3+的物质的量浓度为0.4mol/L,SO42-的物质的量浓度为0.7mol/L,NO3-的物质的量浓度为0.2mol/L,
根据电荷守恒有:3c(Fe3+)+c(Na+)=2c(SO42-)+c(NO3-),
即3×0.4mol/L+c((Na+)=2×0.7mol/L+0.2mol/L,
解得c(Na+)=0.4mol/L,
故选C.
根据电荷守恒有:3c(Fe3+)+c(Na+)=2c(SO42-)+c(NO3-),
即3×0.4mol/L+c((Na+)=2×0.7mol/L+0.2mol/L,
解得c(Na+)=0.4mol/L,
故选C.
点评:本题考查了电荷守恒、物质的量浓度的计算,题目难度不大,注意掌握物质的量浓度概念及计算方法,明确电荷守恒在化学计算中的应用方法.

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
对下列实验的描述不正确的是( )
A、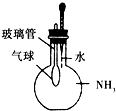 根据气球的变化证明氨气极易溶于水 |
B、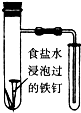 根据小试管中液面的变化判断铁钉发生析氢腐蚀 |
C、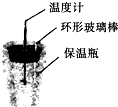 根据温度计读数的变化用稀盐酸和NaOH反应测定中和热 |
D、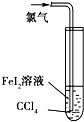 根据试管中液体颜色的变化比较Cl2、Fe3+、I2的氧化性 |
下列说法正的是( )
| A、1 mol 蔗糖可水解生成2 mol葡萄糖 |
| B、CH3-CH=CH-CH3与C3H6一定互为同系物 |
| C、C4H9Cl共有同分异构体9种 |
D、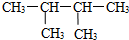 的名称是2,3-二甲基丁烷 的名称是2,3-二甲基丁烷 |
资源利用、环境保护等在与社会可持续发展密切相关的领域发挥着积极作用.下列做法与社会可持续发展理念相违背的是( )
| A、改进汽车尾气净化技术,减少大气污染物的排放 |
| B、过度开采矿物资源,促进地方经济发展 |
| C、开发利用新能源,减少化石燃料的使用 |
| D、加强对工业“三废”的治理,保护环境 |
下列说法正确的是( )
| A、用湿润的碘化钾淀粉试纸检验氯化氢气体中是否混有氯气 |
| B、次氯酸具有酸性,可与碳酸钠反应产生二氧化碳气体 |
| C、新制氯水的酸性一定比久置的氯水强 |
| D、干燥氯气能使有色布条褪色 |
下列事实中,能证明氯化氢是强电解质的是( )
| A、氯化氢易溶于水 |
| B、氯化氢水溶液能导电 |
| C、氯化氢在水溶液中完全电离 |
| D、氯化氢易挥发 |
J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表.已知J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素.下列说法错误的是( )
| J | ||
| R |
| A、J和氢组成的气态氢化物分子中只含有极性共价键 |
| B、M单质能与氢氧化钠溶液反应,产生一种可燃性气体 |
| C、R、T两元素的气态氢化物中,T的气态氢化物更稳定 |
| D、J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4 |