题目内容
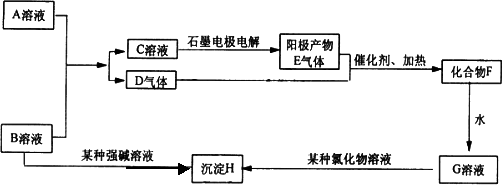
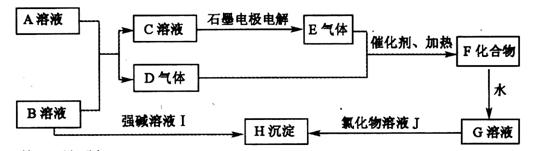
A、B是两种含氧酸的酸式盐溶液,焰色反应均显黄色,D、E均为无色气体,H为不溶于酸的白色沉淀。完成以下问题:
(1)化学式:A____________;B.____________。
(2)C溶液电解时,阳极电极反应方程式_________________。
(3)B溶液与某强碱反应恰好使沉淀后溶液显中性时离子反应方程式_____________________。
(4)A与B溶液混合时发生反应的离子反应方程式____________________________________。
(1)NaHSO3 NaHSO4
(2)4OH--4e-![]() 2H2O+O2↑
2H2O+O2↑
(3) ![]() +2H++Ba2++2OH-
+2H++Ba2++2OH-![]() BaSO4↓+2H2O
BaSO4↓+2H2O
(4) ![]() +H+
+H+![]() SO2↑+H2O
SO2↑+H2O
解析:A、B是两种含氧酸的酸式盐溶液,焰色反应均显黄色,所以A、B均为Na盐,又因为二者能反应生成气体,所用道理为强酸制取弱酸,所以其一必为NaHSO4,因为它在水中可以完全电离出H+,可采取代入法试之,那么结合框图可知B为NaHSO4,A应为弱酸酸式盐NaHSO3,代入可知D为SO2气体,E为O2,F为SO3,G为H2SO4,H为BaSO4沉淀。

| |||||||||||||||||||||||||||||||||