题目内容
工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素.霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾.
(1)大气中的SO2在烟尘的催化下形成硫酸的反应方程式是 .
(2)已知2SO2 (g)+O2 (g)→2SO3(g)△H=-196kJ/mol,提高反应中SO2的转化率,是减少SO2排放的有效措施.
①T温度时,在2L容积固定不变的密闭容器中加入2.0mol SO2和1.0mol O2,5min后反应达到平衡,二氧化硫的转化率为50%,则υ(O2)= .
②在①的条件下,判断该反应达到平衡状态的标志是 (填字母).
a.SO2、O2、SO3三者的浓度之比为2:1:2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2 的生成速率和SO3的生成速率相等
③若反应初始时,在容器中加入1.5mol SO2和0.8molO2,则平衡后二氧化硫的转化率 氧气的转化率(填大于、小于或等)
(1)大气中的SO2在烟尘的催化下形成硫酸的反应方程式是
(2)已知2SO2 (g)+O2 (g)→2SO3(g)△H=-196kJ/mol,提高反应中SO2的转化率,是减少SO2排放的有效措施.
①T温度时,在2L容积固定不变的密闭容器中加入2.0mol SO2和1.0mol O2,5min后反应达到平衡,二氧化硫的转化率为50%,则υ(O2)=
②在①的条件下,判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2:1:2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2 的生成速率和SO3的生成速率相等
③若反应初始时,在容器中加入1.5mol SO2和0.8molO2,则平衡后二氧化硫的转化率
考点:二氧化硫的污染及治理,化学平衡状态的判断,化学平衡的计算,二氧化硫的化学性质
专题:
分析:(1)SO2在烟尘的催化下形成硫酸是2SO2+2H2O+O2=2H2SO4;
(2)①根据三段式求出转化量,再根据反应速率的定义式计算;
②化学平衡的标志是正逆反应速率相同,各组分含量保持不变;
③依据化学平衡影响因素和平衡移动原理分析判断;
(2)①根据三段式求出转化量,再根据反应速率的定义式计算;
②化学平衡的标志是正逆反应速率相同,各组分含量保持不变;
③依据化学平衡影响因素和平衡移动原理分析判断;
解答:
解:(1)SO2在烟尘的催化下形成硫酸是2SO2+2H2O+O2=2H2SO4,故答案为:2SO2+2H2O+O2=2H2SO4;
(2)①T1温度时,在2L的密闭容器中加入4.0molSO2和2.0molO2,5min后反应达到平衡,二氧化硫的转化率为50%,
2SO2(g)+O2?2SO3(g)△H<0
起始量(mol) 2.0 1.0 0
变化量(mol)2.0×50% 0.5 0.5
平衡量(mol) 1.0 0.5 0.5
前5min内O2的平均反应速率=
=0.05mol/(L?min);
故答案为:0.05mol/(L?min);
②化学平衡的标志是正逆反应速率相同,各组分含量保持不变;
a.物质的浓度关系和起始量和转化率有关,SO2、O2、SO3三者的浓度之比为2:1:2 不能说明反应达到平衡状态,故a不符合;
b.因为该反应为气体物质的量增大的反应,恒温恒容条件下,压强为变量,当容器中气体的压强不变说明达到平衡状态,故b符合;
c.反应前后气体质量不变,容器体积不变,密度在反应过程中和平衡状态都不变,容器中混合气体的密度保持不变不能说明费用达到平衡状态,故c不符合;
d.SO3的物质的量不再变化,能说明反应达到平衡状态,故d符合;
e.SO2的生成速率和SO3的生成速率相等说明正逆反应速率相同,能说明反应达到平衡状态,故e符合;
故答案为:bde;
③若反应初始时,在容器中加入1.5mol SO2和0.75mol O2,两者的转化率相等,而现在相当于充入氧气,二氧化硫的转化率增加,而氧气转化率变小,故答案为:大于;
(2)①T1温度时,在2L的密闭容器中加入4.0molSO2和2.0molO2,5min后反应达到平衡,二氧化硫的转化率为50%,
2SO2(g)+O2?2SO3(g)△H<0
起始量(mol) 2.0 1.0 0
变化量(mol)2.0×50% 0.5 0.5
平衡量(mol) 1.0 0.5 0.5
前5min内O2的平均反应速率=
| ||
| 5min |
故答案为:0.05mol/(L?min);
②化学平衡的标志是正逆反应速率相同,各组分含量保持不变;
a.物质的浓度关系和起始量和转化率有关,SO2、O2、SO3三者的浓度之比为2:1:2 不能说明反应达到平衡状态,故a不符合;
b.因为该反应为气体物质的量增大的反应,恒温恒容条件下,压强为变量,当容器中气体的压强不变说明达到平衡状态,故b符合;
c.反应前后气体质量不变,容器体积不变,密度在反应过程中和平衡状态都不变,容器中混合气体的密度保持不变不能说明费用达到平衡状态,故c不符合;
d.SO3的物质的量不再变化,能说明反应达到平衡状态,故d符合;
e.SO2的生成速率和SO3的生成速率相等说明正逆反应速率相同,能说明反应达到平衡状态,故e符合;
故答案为:bde;
③若反应初始时,在容器中加入1.5mol SO2和0.75mol O2,两者的转化率相等,而现在相当于充入氧气,二氧化硫的转化率增加,而氧气转化率变小,故答案为:大于;
点评:本题考查了化学反应速率的计算、化学平衡的判断、电化学等,试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用所学知识解决实际问题的能力.

练习册系列答案
相关题目
能用于治疗胃酸过多的是( )
| A、胃舒平[主要成分Al(OH)3] |
| B、阿司匹林 |
| C、青霉素 |
| D、烧碱 |
将钠、镁、铝各0.3mol,分别放入100mL 1mol?L-1的硫酸中,同温同压下产生的气体的体积比是( )
| A、1:2:3 |
| B、6:3:2 |
| C、3:2:2 |
| D、3:1:1 |
把V L含有KCl和BaCl2的混合溶液分成两等份,一份加入含a mol AgNO3的溶液,恰好使Cl-完全沉淀为AgCl;另一份加入含b mol Na2SO4的溶液,恰好使Ba2+完全沉淀为BaSO4.则原混合溶液中钾离子的浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
可逆反应N2(g)+3H2(g )?2NH3(g),在500℃时,将2mol N2和2mol H2充入容积为10L的密闭容器中进行反应,达到平衡时,NH3不可能达到的浓度是( )
| A、0.08mol?L-1 |
| B、0.12 mol?L-1 |
| C、0.05 mol?L-1 |
| D、0.14mol?L-1 |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O发生反应:CO(g)+H2O(g)?CO2+H2(g),反应在t2时达到平衡,
下列说法不正确的是( )
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.40 | |
| t2 | 0.80 |
| A、反应在t1min内的平均速率为v(H2)=(0.10/t1 )mol?L-1?min-1 |
| B、保持其他条件不变,向平衡体系中再通入0.60 molCO和1.20 molH2O,到达平衡时,c(CO2)=0.90 mol?L-1 |
| C、保持其他条件不变,向平衡体系中再通入0.20 mol H2O(g),与原平衡相比,达到新平衡时CO转化率增大 |
| D、温度升至850℃,上述反应的平衡常数变为0.85,则该反应的正反应为放热反应 |
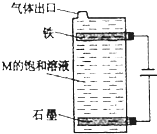 甲、乙、丙、丁、戊、己为原子序数依次增大的短周期主族元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,乙元素最高化合价与最低价的代数和为0;丙、丁、戊的最高价氧化物的水化物之间都能发生反应.用化学用语回答下列问题:
甲、乙、丙、丁、戊、己为原子序数依次增大的短周期主族元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,乙元素最高化合价与最低价的代数和为0;丙、丁、戊的最高价氧化物的水化物之间都能发生反应.用化学用语回答下列问题: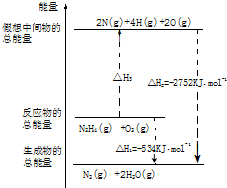 氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用.
氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用.