题目内容
相同条件下,相同物质的量浓度的下列八种溶液:①Na2CO3 ②NaClO ③NaAc ④Na2SO4 ⑤NaHCO3 ⑥NaOH ⑦(NH4)2SO4 ⑧NaHSO4等溶液,pH值由大到小的顺序为: .
考点:盐类水解的应用
专题:基本概念与基本理论,盐类的水解专题
分析:先将物质的按照碱、盐、酸的顺序分类,再根据盐的水解和弱电解质的电离特点比较pH,再按照溶液的pH由大到小进行排序.
解答:
解:属于碱的为:⑥NaOH,显强碱性;
水解呈碱性的为:①Na2CO3 ②NaClO ③NaAc ⑤NaHCO3,对应的酸的酸性越弱,其盐的水解程度越大,pH越大,则pH:①>②>⑤>③;
溶液呈中性的为:④Na2SO4;
溶液呈酸性的有:⑦(NH4)2SO4 ⑧NaHSO4,其中⑦(NH4)2SO4溶液中铵根离子水解显酸性,⑧NaHSO4 溶液中完全电离相当于一元强酸,浓度相同时,溶液的pH:⑧<⑦;
综合以上分析可知,溶液的pH由大到小的顺序是为⑥①②⑤③④⑦⑧,
故答案为:⑥①②⑤③④⑦⑧.
水解呈碱性的为:①Na2CO3 ②NaClO ③NaAc ⑤NaHCO3,对应的酸的酸性越弱,其盐的水解程度越大,pH越大,则pH:①>②>⑤>③;
溶液呈中性的为:④Na2SO4;
溶液呈酸性的有:⑦(NH4)2SO4 ⑧NaHSO4,其中⑦(NH4)2SO4溶液中铵根离子水解显酸性,⑧NaHSO4 溶液中完全电离相当于一元强酸,浓度相同时,溶液的pH:⑧<⑦;
综合以上分析可知,溶液的pH由大到小的顺序是为⑥①②⑤③④⑦⑧,
故答案为:⑥①②⑤③④⑦⑧.
点评:本题考查了溶液pH的大小比较,题目难度不大,注意考虑电解质的强弱以及盐类的水解情况,侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
下列物质的水溶液,因为水解而使溶液呈酸性的是( )
| A、NaHSO4 |
| B、NaHCO3 |
| C、AlCl3 |
| D、Na2SO4 |
实验室中要配制2mol/L的NaCl溶液480mL,配制时应选用的容量瓶的规格和应称取的NaCl分别是( )
| A、480 mL、117g |
| B、500mL、58.5g |
| C、480 mL、58.5 g |
| D、500mL、117g |
常温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:下列判断不正确的是( )
| 实验编号 | 起始浓度/(mol?L-1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
| A、实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+) |
| B、实验①反应后的溶液中:c(OH-)=c(H+)+c(HA) |
| C、实验②反应后的溶液中:c(A-)+c(HA)>0.2 mol/L |
| D、实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+) |
下列实验操作中错误的是( )
| A、萃取操作振荡时,要不时打开分液漏斗的活塞放气 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、蒸发时,蒸发皿必须要垫石棉网加热 |
| D、分液漏斗在使用前要检查是否漏液 |
对于蒸馏实验中的下列说法错误的是( )
| A、为了更好地控制蒸汽温度,应将温度计向下插入接近液面处 |
| B、为了防止暴沸,在对液体混合物进行蒸馏操作时应该加入沸石 |
| C、为了保证冷凝效果,冷凝水应从冷凝管的下口流入上口流出 |
| D、牛角管的作用是使冷凝后的液体沿着其方向流入锥形瓶 |
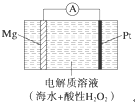 美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )
美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )| A、电池的负极反应为Mg-2e-═Mg2+ |
| B、电池工作时,H+向负极移动 |
| C、电池工作一段时间后,溶液的pH增大 |
| D、电池总反应式是Mg+H2O2+2H+═Mg2++2H2O |