题目内容
x、Y、Z、W、Q是原子序数小于36的常见元素,其相关信息如下表
(1)W位于元素周期表第 周期第 族,其基态原子最外层有 个电子.
(2)X、Y、Z的电负性由小到大的顺序是 .X的氢化物的稳定性比Y的 (填“强”或“弱”),XY2与ZY2中硬度较小的是 (填化学式).
(3)写出工业上用ZY2与X反应制备Z单质的化学方程式 .
(4)在X、Y与氢三种元素组成的多种分子中,有些分子的核磁共振氢谱显示有三种氢,且数目比为1:2:3,写出其中一种分子的名称: .X、Y、Q可以按1:2:1形成一种二元弱酸盐,写出该盐水解的离子方程式: .
| 元素 | 相关信息 |
| X | X原子核外最外层电子数是内层电子数的2倍 |
| Y | Y与X同周期,其基态原于占据s轨道的电子数与占据p轨道的电子数相同 |
| Z | Z是X的同族相邻元素 |
| W | 原子序数为29 |
| Q | Q与Z同周期,且在该周期所有元素中原子半径最大 |
(2)X、Y、Z的电负性由小到大的顺序是
(3)写出工业上用ZY2与X反应制备Z单质的化学方程式
(4)在X、Y与氢三种元素组成的多种分子中,有些分子的核磁共振氢谱显示有三种氢,且数目比为1:2:3,写出其中一种分子的名称:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X原子核外最外层电子数是内层电子数的2倍,则X为C元素,Y与X同周期,其基态原于占据s轨道的电子数与占据p轨道的电子数相同,则Y为O元素,Z是X的同族相邻元素,则Z为Si元素,Q与Z同周期,且在该周期所有元素中原子半径最大,则Q为Na元素,W原子序数为29,则W为Cu元素,据此答题;
解答:
解:X原子核外最外层电子数是内层电子数的2倍,则X为C元素,Y与X同周期,其基态原于占据s轨道的电子数与占据p轨道的电子数相同,则Y为O元素,Z是X的同族相邻元素,则Z为Si元素,Q与Z同周期,且在该周期所有元素中原子半径最大,则Q为Na元素,W原子序数为29,则W为Cu元素,
(1)铜元素位于周期表的第四周期第ⅠB族,其基态原子的价电子排布式为3d104s1,所以它的最外层有1个电子,故答案为:四;ⅠB;1;
(2)X、Y、Z分别为C、O、Si,根据元素周期律,同周期元素从左向右,电负性逐渐增大,氢化物的稳定性逐渐减弱,在同一主族中,从上向下电负性逐渐减小,所以C、O、Si的电负性由小到大的顺序是Si<C<O,C的氢化物的稳定性比O的弱,CO2为分子晶体,硬度小,SiO2为原子晶体,硬度大,
故答案为:Si<C<O;弱;CO2;
(3)工业上用SiO2与C反应制备Si单质的化学方程式为SiO2+C
Si+2CO↑,故答案为:SiO2+C
Si+2CO↑;
(4)C、H、O三种元素组成的分子中,核磁共振氢谱显示有三种氢,且数目比为1:2:3,其分子式为CH3CH2OH,即为乙醇,C、O、Na按1:2:1形成一种二元弱酸盐为Na2C2O4,其水解的离子方程式为C2O42-+H2O?HC2O4-+OH-,故答案为:C2O42-+H2O?HC2O4-+OH-;
(1)铜元素位于周期表的第四周期第ⅠB族,其基态原子的价电子排布式为3d104s1,所以它的最外层有1个电子,故答案为:四;ⅠB;1;
(2)X、Y、Z分别为C、O、Si,根据元素周期律,同周期元素从左向右,电负性逐渐增大,氢化物的稳定性逐渐减弱,在同一主族中,从上向下电负性逐渐减小,所以C、O、Si的电负性由小到大的顺序是Si<C<O,C的氢化物的稳定性比O的弱,CO2为分子晶体,硬度小,SiO2为原子晶体,硬度大,
故答案为:Si<C<O;弱;CO2;
(3)工业上用SiO2与C反应制备Si单质的化学方程式为SiO2+C
| ||
| ||
(4)C、H、O三种元素组成的分子中,核磁共振氢谱显示有三种氢,且数目比为1:2:3,其分子式为CH3CH2OH,即为乙醇,C、O、Na按1:2:1形成一种二元弱酸盐为Na2C2O4,其水解的离子方程式为C2O42-+H2O?HC2O4-+OH-,故答案为:C2O42-+H2O?HC2O4-+OH-;
点评:本题主要考查了元素的位、构、性之间的关系,中等难度,解题时注意根据元素原子的结构特点推断元素的种类.

练习册系列答案
相关题目
将下列各组物质按单质、氧化物、酸、碱、盐分类顺序排列,其中正确的是( )
| A、水银、干冰、硫酸、苛性钠、镁铝合金 |
| B、碘酒、冰、盐酸、烧碱、食盐 |
| C、氢气、二氧化硫、硝酸、纯碱、胆矾 |
| D、铜、氧化铜、醋酸、熟石灰、醋酸铵 |
 某学习小组探究溴乙烷的消去反应并验证产物.
某学习小组探究溴乙烷的消去反应并验证产物.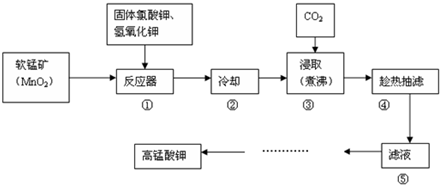
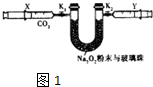 (1)如图1注射器X中抽取100mL CO2,U形管中装有适量小玻璃珠和约1.5gNa2O2粉末,打开K1、K2止水夹,缓缓将CO2压至U形管中,观察到的实验现象是
(1)如图1注射器X中抽取100mL CO2,U形管中装有适量小玻璃珠和约1.5gNa2O2粉末,打开K1、K2止水夹,缓缓将CO2压至U形管中,观察到的实验现象是