题目内容
Harbermann等设计出利用Desulfovibrio desulfurcan菌种生成的硫化物作为介体的微生物燃料电池,电池内部有质子(即H+)通过,该系统不经任何维护可连续运行5年.该电池的负极反应式为S2-+4H2O-8e-=SO42-+8H+.下列说法中正确的是( )
| A、若有1.12 L氧气参与反应,则有0.2 mol电子发生转移 |
| B、质子由正极移向负极 |
| C、该电池的总反应为S2-+2O2=SO42- |
| D、正极的电极反应式为2O2+8e-+4H2O=8OH- |
考点:化学电源新型电池
专题:电化学专题
分析:A、根据化合价的变化确定电子的转移情况;
B、根据原电池中离子的移动方向来回答判断;
C、根据电池反应=负极+正极来书写总反应;
D、在原电池的正极上发生得电子的还原反应.
B、根据原电池中离子的移动方向来回答判断;
C、根据电池反应=负极+正极来书写总反应;
D、在原电池的正极上发生得电子的还原反应.
解答:
解:A、微生物燃料电池的正极反应为:O2+4e-+4H+=2H2O,若有标况下1.12 L即0.05mol氧气参与反应,才有0.2 mol电子发生转移,故A错误;
B、根据原电池中离子的移动方向知道:质子由负极移向正极,故B错误;
C、该电池的负极反应式为S2-+4H2O-8e-=SO42-+8H+,正极反应为:O2+4e-+4H+=2H2O,该电池的总反应为S2-+2O2=SO42-,故C正确;
D、微生物燃料电池的正极反应为:O2+4e-+4H+=2H2O,故D错误.
故选C.
B、根据原电池中离子的移动方向知道:质子由负极移向正极,故B错误;
C、该电池的负极反应式为S2-+4H2O-8e-=SO42-+8H+,正极反应为:O2+4e-+4H+=2H2O,该电池的总反应为S2-+2O2=SO42-,故C正确;
D、微生物燃料电池的正极反应为:O2+4e-+4H+=2H2O,故D错误.
故选C.
点评:本题考查学生原电池的工作原理以及电极反应式的书写知识,注意教材知识的梳理和掌握,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
从物质分类的角度看,下列说法错误的是( )
| A、石油属于混合物 |
| B、氮气属于单质 |
| C、甲烷属于化合物 |
| D、干冰属于有机物 |
把aL硫酸铵和硝酸铵的混合液分成两等份,一份加入bmol 烧碱并加热,刚好把NH3 全部赶出.另一份需消耗cmolBaCl2,沉淀反应刚好完全,原溶液中硝酸根离子的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
煤、石油、天然气是当今世界上最重要的化石燃料,下列关于它们的描述不正确的是( )
| A、燃烧时都会放出热量 |
| B、都是混合物 |
| C、都是重要的化工原料 |
| D、都是可再生能源 |
下列说法不正确的是( )
| A、反应C(s)+CO2(g)=2CO(g)△H>0,在任何条件下均不能自发进行 |
| B、铅蓄电池在放电过程中,溶液的pH值增加 |
| C、常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小 |
| D、温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变 |
常温下,在10mL 0.2mol/L某一元强酸HA的溶液中逐滴加入a mL 0.1mol/L的氨水,下列有关说法中正确的是( )
| A、当c(NH4+)=c(A-)时,a一定等于20 |
| B、当c(NH4+)>c(A-)时,a一定大于20 |
| C、当c(H+)=c(OH-)时,a一定小于20 |
| D、当pH=7时,c(NH4+)=c(A-)=c(H+)=c(OH-) |
下列化学实验基本操作中,正确的是( )
| A、稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的量筒中并搅拌 |
| B、用量筒量取液体时,视线与量筒内液体保持水平 |
| C、用滴管滴加液体时,为防止液滴飞溅,滴管紧贴试管内壁 |
| D、用托盘天平称量物质时,称量物放在左盘,砝码放在右盘 |
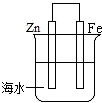 如图是模拟铁的电化学防护装置.以下叙述正确的是( )
如图是模拟铁的电化学防护装置.以下叙述正确的是( )| A、此装置属于电解池 |
| B、此装置中的铁极上发生氧化反应 |
| C、该电化学防护法称为“牺牲阳极阴极保护法” |
| D、该电化学防护法称为“外加电源阴极保护法” |