题目内容
20.下列说法正确的是( )| A. | 铁表面镀铜时,铁与电源的正极相连,铜与电源的负极相连 | |
| B. | 向氨水中不断通入CO2,随着CO2的增加,$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$不断增大 | |
| C. | 3C(s)+CaO(s)=CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的△H>0 | |
| D. | 合成氨时,其他条件不变升高温度,反应速率v(H2)和氢气的平衡转化率均增大 |
分析 A.电镀池中,作阳极的是镀层金属,做阴极的是待镀金属;
B.向氨水中不断通入CO2,一水合氨浓度减小,铵根离子浓度增大,结合电离常数分析;
C.根据反应自发进行的判断依据△H-T△S<0分析解答;
D.合成氨反应为放热反应.
解答 解:A.在铁件的表面镀铜的电镀池中,作阳极的是镀层金属铜,与电源的正极相连,阳极上金属铜失电子发生氧化反应,阴极上铜离子得电子生成铜单质,铁与电源的负极相连做阴极,故A错误;
B.向氨水中不断通入CO2,一水合氨浓度减小,铵根离子浓度增大,由于$\frac{c(N{{H}_{4}}^{+})×c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$是常数,所以$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$不断减小,故B错误;
C.3C(s)+CaO(s)=CaC2(s)+CO(g)在常温下不能自发进行,已知△S>0,由△H-T△S<0可知,说明该反应的△H>0,故C正确;
D.合成氨反应为放热反应,升高温度反应速率加快,平衡逆向移动,所以氢气的转化率减小,故D错误;
故选C.
点评 本题考查了电镀原理的应用、弱电解质的电离、反应自发进行的判断以及化学平衡的影响因素等知识点,题目难度中等,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
5.对25℃时的醋酸溶液,若采用下列不同的措施,能使醋酸电离度增大的是( )
| A. | 加入NaOH固体 | B. | 加入醋酸钠晶体 | C. | 加入盐酸 | D. | 降温 |
9.常温下,将pH=11的氨水与pH=3的盐酸等体积混合,充分反应后溶液的pH( )
| A. | 小于7 | B. | 等于7 | C. | 大于7 | D. | 无法判断 |
10.聚2-甲基-1-丙烯是生产汽油清洁剂(kerocom piba)的中间产物.下列关于聚异丁烯的说法中,错误的是( )
| A. | 聚2-甲基-1-丙烯可以通过加聚反应制得 | |
| B. | 聚2-甲基-1-丙烯的分子式为 (C4H8)n | |
| C. | 聚2-甲基-1-丙烯完全燃烧生成CO2和H2O的物质的量相等 | |
| D. | 聚2-甲基-1-丙烯能使溴的四氯化碳溶液褪色 |
 实验室配制500mL 0.5mol•L-1的NaCl溶液,有如下操作步骤:
实验室配制500mL 0.5mol•L-1的NaCl溶液,有如下操作步骤: lCl3溶液
lCl3溶液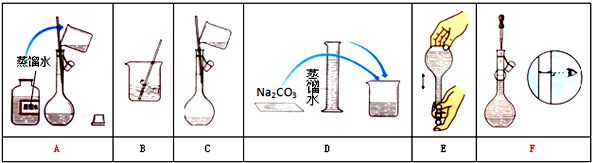
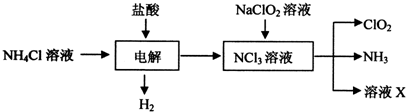
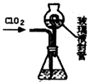 二氧化氯(C1O2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水.实验室可用Fa-14Cl、盐酸、NaCl02(亚氯酸钠)为原料制备C1O2的流程如下:
二氧化氯(C1O2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水.实验室可用Fa-14Cl、盐酸、NaCl02(亚氯酸钠)为原料制备C1O2的流程如下: