题目内容
常温下,将c1 mol?L-1的盐酸和c2 mol?L-1的氨水等体积混合,下列叙述错误的是( )
| A、c(NH4+)+c(H+)═c(Cl-)+c(OH-) |
| B、当c1=c2时,c(NH4+)+c(NH3?H2O)═c(Cl-) |
| C、当pH=7,一定是C2>C1 |
| D、当pH<7,一定是C1=C2 |
考点:酸碱混合时的定性判断及有关ph的计算,离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:A、依据电荷守恒分析;
B、依据溶液中存在的物料守恒分析,当c1=c2时盐酸和氨水物质的量相等;
C、pH=7溶液呈中性氨水物质的量应大于盐酸的物质的量;
D、当pH<7时溶液显酸性,满足c1=c2或c1>c2.
B、依据溶液中存在的物料守恒分析,当c1=c2时盐酸和氨水物质的量相等;
C、pH=7溶液呈中性氨水物质的量应大于盐酸的物质的量;
D、当pH<7时溶液显酸性,满足c1=c2或c1>c2.
解答:
解:A、依据电荷守恒分析,溶液中离子存在电荷守恒c(NH4+)+c(H+)═c(Cl-)+c(OH-),故A正确;
B、依据溶液中存在的物料守恒分析,当c1=c2时盐酸和氨水物质的量相等,溶液中物料守恒为:c(NH4+)+c(NH3?H2O)═c(Cl-),故B正确;
C、pH=7溶液呈中性,氨水物质的量应大于盐酸的物质的量,一定是c2>c1,故C正确;
D、当pH<7时溶液显酸性,恰好反应生成氯化铵溶液显酸性满足c1=c2,盐酸过量满足c1>c2,故D错误;
故选D.
B、依据溶液中存在的物料守恒分析,当c1=c2时盐酸和氨水物质的量相等,溶液中物料守恒为:c(NH4+)+c(NH3?H2O)═c(Cl-),故B正确;
C、pH=7溶液呈中性,氨水物质的量应大于盐酸的物质的量,一定是c2>c1,故C正确;
D、当pH<7时溶液显酸性,恰好反应生成氯化铵溶液显酸性满足c1=c2,盐酸过量满足c1>c2,故D错误;
故选D.
点评:本题考查了电解质溶液中电荷守恒、物料守恒的分析判断,注意酸碱反应定量关系的计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
四种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,X2+和Z-离子的电子数之差为8.下列说法不正确的是( )
| A、与W相邻的同主族元素可制成重要的半导体材料 |
| B、元素原子半径从大到小的顺序是X、Y、Z |
| C、W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是H2YO4 |
| D、X的单质在W的最高价氧化物中的燃烧反应属于置换反应 |
分离饱和食盐水与沙子的混合物,可选用的分离方法为( )
| A、萃取分液法 | B、加热分解法 |
| C、蒸馏法 | D、过滤法 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、使苯酚显紫色的溶液:NH4+、K+、SCN-、NO3- |
| B、澄清透明的溶液:Cu2+、Mg2+、SO42-、Cl- |
| C、0.1mol?L-1 Na2CO3溶液:NH4+、Fe2+、SO42-、NO3- |
| D、c(Fe2+)=1.0 mol?L-1溶液:H+、K+、Cl-、MnO4- |
在实验室中,对下列事故或药品的处理正确的是( )
| A、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| B、若实验室发生漏电着火时,应用大量水灭火 |
| C、实验后,剩余的药品不能放回原瓶,应放在指定位置 |
| D、含硫酸的废液倒入水槽,用水冲入下水道 |
已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH:则下列说法或表达正确的是( )
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| PH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A、CO2+H2O+2NaClO═Na2CO3+2HClO |
| B、2HCN+Na2CO3═CO2+2NaCN+H2O |
| C、常温下电离常数比较:Ka (H2CO3)>Ka(CH3COOH)>Ka(C6H5OH) |
| D、结合质子能力由强到弱的顺序为:CO2-3>HCO-3>CH3COO- |
下列醇中能由醛还原制得的是( )
| A、CH3CH2CH2OH |
| B、(CH3)2CHCH(CH3)OH |
| C、(CH3)3COH |
| D、(CH3)2CHOH |
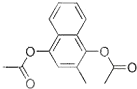 维生素k4是核酸的组成成分,在体内参与RNA和DNA合成.可用来治疗肿瘤病人因化疗或放疗等引起的白细胞减少.下列有关维生素k4说法正确的是
维生素k4是核酸的组成成分,在体内参与RNA和DNA合成.可用来治疗肿瘤病人因化疗或放疗等引起的白细胞减少.下列有关维生素k4说法正确的是