题目内容
6.用NA表示阿伏加德罗常数,下列叙述中正确的是( )| A. | 100 mL 0.1 mol•L-1稀硫酸中含有硫酸根个数为0.1NA | |
| B. | 常温下,1.12 L氮气所含原子数为0.1NA | |
| C. | 1 mol Na2O2与足量的盐酸反应,转移电子数为2NA | |
| D. | 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA |
分析 A.根据n=cV计算出硫酸的物质的量,硫酸为强电解质,根据N=nNA计算出含有硫酸根离子的数目;
B.常温下,不是标准状况下;
C.1mol过氧化钠与足量盐酸反应生成0.5mol氧气,过氧化钠中氧元素的化合价为-1价,据此计算转移电子数;
D.二者最简式为NO2,根据最简式计算混合物中含有原子的物质的量及数目.
解答 解:A.100 mL 0.1mol•L-1稀硫酸中含有0.01mol硫酸,硫酸为强电解质,则溶液中含有0.1mol硫酸根离子,含有硫酸根个数为0.01NA,故A错误;
B.不是标准状况下,不能使用标况下的气体摩尔体积计算,故B错误;
C.1 mol Na2O2与足量的盐酸反应生成0.5mol氧气,转移电子的物质的量为:0.5mol×2=1mol,转移电子数为NA,故C错误;
D.46 gNO2和N2O4混合气体含有46g最简式NO2,含有最简式NO2的物质的量为:$\frac{46g}{46g/mol}$=1mol,1mol最简式NO2中含有3mol原子,含有的原子数为3NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的计算与判断,题目难度不大,明确标况下气体摩尔体积的使用条件为解答关键,注意掌握物质的量与阿伏伽德罗常数、摩尔质量等之间的转化关系,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
2.标况下气体的摩尔体积为( )
| A. | 22.4 | B. | 22.4L | C. | 22.4L/mol | D. | 11.2L |
14.已知漂白液是含有NaClO和NaCl混合溶液(pH>7),下列关于该溶液说法正确的是( )
| A. | 该溶液中,Ag+、K+、NO3?、Mg2+可以大量共存 | |
| B. | 该溶液中,H+、NH4+、SO42?、I?可以大量共存 | |
| C. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023 | |
| D. | 向该溶液中滴入少量Na2SO3溶液,反应的离子方程式为:SO32?+ClO?═Cl?+SO42? |
11.下列常见物质的俗名与化学式对应正确的是( )
| A. | 烧碱--NaOH | B. | 小苏打--Na2SO4 | C. | 熟石灰--CaCl2 | D. | 明矾--Al2(SO4)3 |
18.下列实验事实不能用勒夏特列原理解释的是( )
| A. | 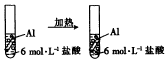 | |||||||||
| B. |
| |||||||||
| C. | 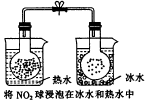 | |||||||||
| D. |
|
15.在四个相同的容器中,在不同的温度下(其它条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是( )
| A. | v(NH3)=0.1 mol/(L•min) | B. | v (N2)=0.6 mol/(L•min) | ||
| C. | v (N2)=0.02mol/(L•s) | D. | v (H2)=0.3 mol/(L•min) |
16.合成导电高分子材料PPV的反应: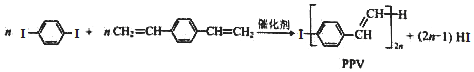
下列说法中正确的是( )
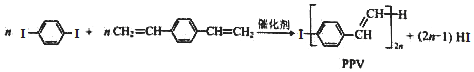
下列说法中正确的是( )
| A. | 合成PPV的反应为加聚反应 | |
| B. | PPV与聚苯乙烯具有相同的重复结构单元 | |
| C. | 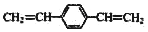 和苯乙烯互为同系物 和苯乙烯互为同系物 | |
| D. | 通过质谱法可测定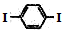 的相对分子质量 的相对分子质量 |
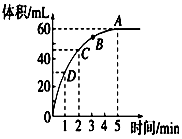 加入0.1mol的MnO2粉末于50mL过氧化氢的溶液中(密度为 1.1g•mL-1),在标准状况下放出气体的体积和时间的关系如图所 示,回答下列问题:
加入0.1mol的MnO2粉末于50mL过氧化氢的溶液中(密度为 1.1g•mL-1),在标准状况下放出气体的体积和时间的关系如图所 示,回答下列问题: