题目内容
下列反应的离子方程式正确的是( )
| A、二氧化硫通入氯化铁溶液:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+ |
| B、Na2CO3水解:CO32-+H2O=H2CO3+2OH- |
| C、硫酸氢铵溶液中滴加少量NaOH溶液:H++NH4++2OH-=NH3?H2O+H2O |
| D、碱性条件下铝粉还原NaNO2:NO2-+2Al+3OH-+H2O=2AlO2-+NH3?H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.三价铁离子具有强的氧化性能够氧化二氧化硫生成硫酸根离子;
B.碳酸根为多元弱酸根离子,分步水解,用可逆号;
C.氢氧化钠少量,只发生氢离子与氢氧根离子的反应;
D.氧原子个数不守恒.
B.碳酸根为多元弱酸根离子,分步水解,用可逆号;
C.氢氧化钠少量,只发生氢离子与氢氧根离子的反应;
D.氧原子个数不守恒.
解答:
解:A.二氧化硫通入氯化铁溶液,离子方程式:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+,故A正确;
B.Na2CO3水解的离子方程式:CO32-+H2O?HCO3-+OH-,故B错误;
C.硫酸氢铵溶液中滴加少量NaOH溶液,离子方程式:H++OH-=H2O,故C错误;
D.碱性条件下铝粉还原NaNO2的离子反应为:NO2-+2Al+OH-+2H2O=2AlO2-+NH3?H2O,故D错误;
故选:A.
B.Na2CO3水解的离子方程式:CO32-+H2O?HCO3-+OH-,故B错误;
C.硫酸氢铵溶液中滴加少量NaOH溶液,离子方程式:H++OH-=H2O,故C错误;
D.碱性条件下铝粉还原NaNO2的离子反应为:NO2-+2Al+OH-+2H2O=2AlO2-+NH3?H2O,故D错误;
故选:A.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意多元弱酸酸根离子分步水解.

练习册系列答案
 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
下列离子方程式书写不正确的是( )
| A、Fe粉投入FeCl3溶液中:Fe+2Fe3+═3Fe2+ |
| B、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| C、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| D、FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
下列说法正确的是( )
| A、NH3是极性分子,分子中N原子处在3个H原子所组成的三角形的中心 |
| B、H2O的熔、沸点大于H2S是由于H2O分子之间存在氢键 |
| C、乙醇分子与水分子之间只存在范德华力 |
| D、氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
| A、S和Si |
| B、CCl4和KCl |
| C、NaCl和HCl |
| D、CO2和H2O |
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、饱和氯水中:Cl-、NO3-、Na+、CO32- |
| B、含大量HCO3-的溶液中:C6H5O-、K+、SO42-、Br- |
| C、水电离出的c(H+)=1.0×10-13 mol?L-1的溶液中:SO42-、K+、Cl-、HSO3- |
| D、使甲基橙显红色的溶液中:NO3-、I-、Na+、Al3+ |
下列各种情况下,溶液中可能大量存在的离子组是( )
| A、澄清透明的溶液中:I-、Cl-、ClO-、Na+ |
| B、由水电离出的c(H+)=1×10-12mol/L的溶液中:K+、Ba2+、OH-、NO-3 |
| C、使pH试纸呈红色的溶液中:K+、Fe2+、NO-3、MnO-4 |
| D、含有大量Fe2+的溶液中:K+、Na+、SO2-3、SO2-4 |
小苏打(碳酸氢钠)是焙制面点的一种常用发酵剂,小苏打属于( )
| A、酸 | B、碱 | C、盐 | D、碱性氧化物 |
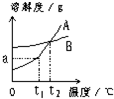 A、B两种固体物质的溶解度曲线如图所示.请回答:
A、B两种固体物质的溶解度曲线如图所示.请回答: