题目内容
12.某学生的实验报告所列出的下列数据中合理的是( )| A. | 用10mL量筒量取7.13mL稀盐酸 | |
| B. | 用pH计测得某稀盐酸的pH为1.54 | |
| C. | 广泛pH试纸润湿后,测得某溶液的pH为2.3 | |
| D. | 用标准的盐酸滴定待测的NaOH溶液时,滴定完毕后,酸式滴定管中盐酸的读数为17.1mL |
分析 A.量筒的精确度为0.1mL;
B.pH计精确到0.01;
C.广泛pH试纸精确到整数;
D.滴定管精确度为0.01.
解答 解:A.量筒的精确度为0.1mL,无法量取7.13 mL稀盐酸,故A错误;
B.PH计精确到0.01,可测得某稀盐酸的pH为1.54,故B正确;
C.广泛pH试纸测得溶液的pH值应是整数,故C错误;
D.滴定管精确度为0.01,读数为17.10mL,故D错误.
故选B.
点评 本题考查化学实验方案的评价,涉及中学化学中常用仪器在使用中读数的问题,难度不大,注意熟悉不同仪器的精确度不同并熟练掌握.

练习册系列答案
相关题目
2.下列关于胶体的叙述正确的是( )
| A. | Fe(OH)3胶体粒子直径在1nm~100 nm之间 | |
| B. | 胶体区别于其他分散系的本质特征是有丁达尔效应 | |
| C. | Fe(OH)3胶体中混有少量FeCl3,可以采取过滤的方法分离 | |
| D. | 将饱和FeCl3溶液滴加到沸水中长时间加热制得Fe(OH)3胶体 |
20.下列叙述正确的是( )
| A. | 浓硫酸有氧化性,稀硫酸没有氧化性 | |
| B. | 稀释浓硫酸时,将浓硫酸沿着量筒壁慢慢注入盛水的量筒中,并不断搅拌 | |
| C. | 硝酸浓度越大氧化能力越强 | |
| D. | 金属和硝酸反应,浓度由浓到稀,对应的还原产物有NO2、NO和H2 |
7.下列有关化学术语或物质变化的说法不正确的是( )
| A. | Na+的结构示意图为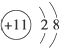 | |
| B. | 明矾的化学式为KAl(SO4)2•12H2O | |
| C. | 某微粒的电子数等于质子数,则该微粒可能是分子或离子 | |
| D. | 化学变化不产生新元素,产生新元素的变化不是化学变化 |
4.分子式为C10H14的芳香烃中,苯环上一溴代物有两种结构的物质共有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
3.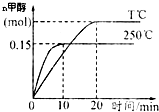 将1molCO和2molH2充入一容积为1L的密闭容器中,分别在250℃、T℃发生反应:CO(g)+2H2(g)?CH3OH(g)△H=akJ/mol,根据图示判断,下列结论正确的是( )
将1molCO和2molH2充入一容积为1L的密闭容器中,分别在250℃、T℃发生反应:CO(g)+2H2(g)?CH3OH(g)△H=akJ/mol,根据图示判断,下列结论正确的是( )
 将1molCO和2molH2充入一容积为1L的密闭容器中,分别在250℃、T℃发生反应:CO(g)+2H2(g)?CH3OH(g)△H=akJ/mol,根据图示判断,下列结论正确的是( )
将1molCO和2molH2充入一容积为1L的密闭容器中,分别在250℃、T℃发生反应:CO(g)+2H2(g)?CH3OH(g)△H=akJ/mol,根据图示判断,下列结论正确的是( )| A. | a<0,T<250 | |
| B. | 250℃时,0~10min内:v(H2)=0.015mol/(L•min) | |
| C. | CO的平衡转化率在250℃时比T℃大 | |
| D. | 250℃时,起始时向容器中改充1molCH3OH气体,恒温达平衡后,CH3OH的物质的量大于0.15mol |
 钛(Ti)被称为继铁、铝之后的第三金属.
钛(Ti)被称为继铁、铝之后的第三金属.