题目内容
13.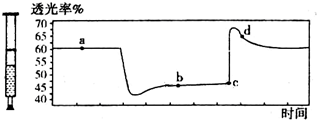 已知2NO2═N2O4+Q (Q>0),将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )
已知2NO2═N2O4+Q (Q>0),将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )| A. | c点的操作是拉伸注射器 | |
| B. | b点与a点相比,c(NO2)增大,c(N2O4)减小 | |
| C. | 若反应在一绝热容器中进行,则a、b两点的平衡常数Ka>Kb | |
| D. | d点:v(正)>v(逆) |
分析 该反应是正反应气体体积减小的放热反应,压强增大平衡虽正向移动,但二氧化氮浓度增大,混合气体颜色变深,压强减小平衡逆向移动,但二氧化氮浓度减小,混合气体颜色变浅,
A.据图分析,c点后透光率增大,c点是拉伸注射器的过程,气体颜色变浅,透光率增大;
B.b点与a点相比,a到b是透光率减小后增加,说明是压缩体积,气体浓度增大,平衡正向进行后略有变浅,但比开始颜色深,所以c(NO2)增大,c(N2O4)增大;
C.若反应在一绝热容器中进行,随反应进行温度不同,平衡常数随之变化,b点气体颜色变深,透光率变小,说明平衡逆向进行,此时温度高;
D.d点是平衡向气体体积增大的逆向移动过程,据此分析.
解答 解:A.c点气体颜色变浅,透光率增大,c点操作是拉伸注射器的过程,故A正确;
B.b点与a点相比,a到b是透光率减小后增加,说明是压缩体积,气体浓度增大,平衡正向进行后略有变浅,二氧化氮和四氧化二氮的浓度都增大,故B错误;
C.若反应在一绝热容器中进行,随反应进行温度不同,平衡常数随之变化,b点气体颜色变深,透光率变小,说明平衡逆向进行,此时温度高,则a、b两点的平衡常数Ka>Kb,故C正确;
D.d点是透光率减小,气体颜色加深,平衡向气体体积增大的逆向移动过程,v(正)<v(逆),故D错误;
故选AC.
点评 本题通过图象和透光率考查了压强对平衡移动的影响,注意勒夏特列原理的应用,题目难度较大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
20.“纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是胶体 ②是溶液 ③能产生丁达尔效应
④不能透过滤纸 ⑤能透过滤纸 ⑥能透过半透膜.
①是胶体 ②是溶液 ③能产生丁达尔效应
④不能透过滤纸 ⑤能透过滤纸 ⑥能透过半透膜.
| A. | ①③⑤ | B. | ②③④ | C. | ②③⑤ | D. | ①③⑤⑥ |
1.某澄清溶液,可能含有NH4+、Na+、Cl-、CO32-、I-中的一种或几种,现做如下实验:
①通入足量氯气,溶液变为棕黄色,滴加淀粉溶液后溶液显蓝色
②加入BaCl2有白色沉淀生成,再加入足量盐酸后,沉淀完全溶解,并有气体生成
③用铂丝蘸取少量溶液做焰色反应实验,火焰的颜色呈黄色
④加入NaOH溶液并加热,没有任何现象
下列关于该澄清溶液的说法中错误的是( )
①通入足量氯气,溶液变为棕黄色,滴加淀粉溶液后溶液显蓝色
②加入BaCl2有白色沉淀生成,再加入足量盐酸后,沉淀完全溶解,并有气体生成
③用铂丝蘸取少量溶液做焰色反应实验,火焰的颜色呈黄色
④加入NaOH溶液并加热,没有任何现象
下列关于该澄清溶液的说法中错误的是( )
| A. | 一定含有I- | B. | 一定含有CO32- | C. | 一定含有NH4+ | D. | 一定含有Na+ |
18.下列说法不正确的是( )
| A. | 原电池外电路中电子由负极流向正极 | |
| B. | 原电池中发生还原反应的电极是正极 | |
| C. | 电解池中发生还原反应的电极是阳极 | |
| D. | 电解池中质量增加的电极是阴极 |
5.对于某些离子的检验及结论正确的是( )
| A. | 向某溶液中滴加NaOH溶液并加热,用湿润的蓝色石蕊试纸于试管口以检验NH4+ | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加入盐酸,沉淀不消失,一定有SO42- | |
| C. | 某待测液焰色反应呈黄色,则待测液中一定不含有K+ | |
| D. | 某溶液中加入KSCN后,溶液无变化,再加入H2O2后,溶液变成血红色,说明原溶液中一定含有Fe2+ |
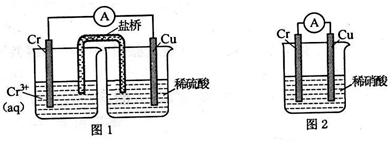 铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各 种性能的不锈钢,CrO3大量地用于电镀工业中.
铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各 种性能的不锈钢,CrO3大量地用于电镀工业中.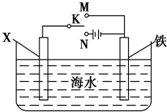 ,可以模拟铁的电化学防护.若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于N处.若 X 为锌,开关K 置于N或M处.
,可以模拟铁的电化学防护.若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于N处.若 X 为锌,开关K 置于N或M处.