题目内容
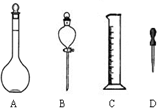
配制一定物质的量浓度的NaOH溶液,下列叙述正确的是( )
| A、称量时,将NaOH固体直接放在托盘天平的左盘上 |
| B、将NaOH固体在烧杯中溶解后立即转移至容量瓶中 |
| C、定容时,俯视容量瓶的刻度线会使所配溶液的浓度偏高 |
| D、定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线 |
考点:溶液的配制
专题:实验评价题
分析:A、NaOH固体易潮解,应放到小烧杯里称量;
B、NaOH固体溶于水放热;
C、根据c=
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
D、定容摇匀后发现溶液体积低于刻度线是正常的.
B、NaOH固体溶于水放热;
C、根据c=
| n |
| V |
D、定容摇匀后发现溶液体积低于刻度线是正常的.
解答:
解:A、NaOH固体易潮解,应放到小烧杯里称量,不能直接放到托盘上,故A错误;
B、NaOH固体溶于水放热,故应冷却至室温后再移液,故B错误;
C、定容时,俯视容量瓶的刻度线会使所配溶液的体积偏小,则浓度偏高,故C正确;
D、定容摇匀后发现溶液体积低于刻度线是正常的,若再加水至刻度线,则浓度会偏小,故D错误.
故选C.
B、NaOH固体溶于水放热,故应冷却至室温后再移液,故B错误;
C、定容时,俯视容量瓶的刻度线会使所配溶液的体积偏小,则浓度偏高,故C正确;
D、定容摇匀后发现溶液体积低于刻度线是正常的,若再加水至刻度线,则浓度会偏小,故D错误.
故选C.
点评:本题考查了一定物质的量浓度溶液的配制过程中的操作和误差分析,难度不大,掌握实验方法是解题关键.

练习册系列答案
相关题目
在0.1mol?L-1的醋酸溶液中,存在电离平衡CH3COOH?CH3COO-+H+,如果要使平衡向逆反应方向移动,同时增大c(H+),应采用的方法是( )
| A、加入0.01 mol?L-1的CH3COOH溶液 |
| B、加入CH3COONa固体 |
| C、稀释 |
| D、加入浓盐酸 |
下列实验方法正确的是( )
| A、向无色溶液中加入氯化钡溶液有白色沉淀出现,再加入盐酸,沉淀不消失,则溶液中一定含有SO42- |
| B、用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中可能含有K+ |
| C、用CCl4萃取碘水后分液时,先打开分液漏斗活塞,放出下层液体,再关闭活塞,更换烧杯后继续打开分液漏斗活塞,放出上层液体 |
| D、检验某溶液中是否含有Fe2+时,可先加入适量的氯水,再滴加硫氰化钾溶液,若溶液变为红色,则说明溶液中一定含有Fe2+ |
下列关于“纯碱”的分类正确的是( )
| A、酸 | B、碱 | C、盐 | D、电解质 |
下列溶液中,与200mL 0.5mol/L Na2SO4溶液所含的Na+ 物质的量浓度相同的是( )
| A、200 mL 0.25 mol/L NaCl溶液 |
| B、200 mL 1 mol/L NaCl溶液 |
| C、100 mL 0.5 mol/L NaOH溶液 |
| D、100 mL 2 mol/L NaOH溶液 |
 烧杯中装有100mLH2SO4和Na2SO4的混合液,其浓度分别为0.16mol/L和2mol/L,欲使其浓度分别变为1.6mol/L和0.2mol/L,在只有蒸馏水和18mol/L浓H2SO4以及必要仪器的条件下,完成任务:
烧杯中装有100mLH2SO4和Na2SO4的混合液,其浓度分别为0.16mol/L和2mol/L,欲使其浓度分别变为1.6mol/L和0.2mol/L,在只有蒸馏水和18mol/L浓H2SO4以及必要仪器的条件下,完成任务: