题目内容
15.完成下列反应的化学方程式或离子方程式:(1)铁粉与水蒸气反应化学方程式:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(2)铝与氢氧化钠溶液反应化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
(3)锌粒与氯化铜溶液反应离子方程式:Zn+Cu2+═Zn2++Cu.
分析 (1)高温条件下,铁和水蒸气反应生成四氧化三铁和氢气;
(2)Al和NaOH溶液反应生成偏铝酸钠和氢气;
(3)Zn和氯化铜发生置换反应生成Cu和氯化锌.
解答 解:(1)高温条件下,铁和水蒸气反应生成四氧化三铁和氢气,反应方程式为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(2)Al和NaOH溶液反应生成偏铝酸钠和氢气,离子方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
(3)Zn和氯化铜发生置换反应生成Cu和氯化锌,离子方程式为Zn+Cu2+═Zn2++Cu,故答案为:Zn+Cu2+═Zn2++Cu.
点评 本题考查离子方程式和化学方程式的书写,明确反应实质是解本题关键,知道离子方程式书写规则,注意Fe和水常温下不反应,高温下发生置换反应,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.设NA为阿伏加德罗常数的值,则下列说法不正确的是( )
| A. | 14g乙烯和环丙烷混合物中含有的碳原子数目为NA | |
| B. | 1.6g甲烷完全燃烧生成二氧化碳和水,转移的电子数为0.8NA | |
| C. | 0.1mol乙炔分子中含有的共用电子对数目为0.5NA | |
| D. | 在标准状态下,2.24L己烷含有的氢原子数目为1.4NA |
10.下列有关表示正确的是( )
| A. | 过氧化钙(CaO2)的电子式: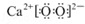 | |
| B. | 某微粒的结构示意简图为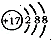 ,则该元素在周期表中位于第三周期、VIA族 ,则该元素在周期表中位于第三周期、VIA族 | |
| C. | H2CO3的电离方程式:H2CO3?2H++CO32- | |
| D. | 葡萄糖的结构简式:C6H12O6 |
20.现有浓度均为1mol/L的四种溶液:①HCl,②NaOH,③CH3COOH,④NH4Cl,由水电离出的C(H+)大小关系正确的是( )
| A. | ④>③>①=② | B. | ①=②>③>④ | C. | ②>①>③>④ | D. | ④>③>①>② |
7.下列离子方程式书写正确的是( )
| A. | Na2CO3水解:CO32-+2H2O?H2CO3+2OH- | |
| B. | 用惰性电极电解饱和NaCl溶液:2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$ Cl2↑+H2↑+2OH- | |
| C. | FeBr2溶液中通入足量的Cl2:2Fe2++Cl2=2Fe3++2Cl- | |
| D. | 等体积等物质的量浓度的Ca(HCO3)2与NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
4.有一块铝铁合金,将其溶解于足量盐酸中,再加入过量NaOH溶液,在空气中静置至红褐色沉淀不再增加时,将沉淀滤出再灼烧至恒重,得到残留物的质量与原合金质量相同,则合金中铝的质量分数( )
| A. | 52.4% | B. | 30% | C. | 70% | D. | 47.6% |
5. 中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用.有机物M是中药狼把草的成分之一,其结构如图所示.下列叙述不正确的是( )
中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用.有机物M是中药狼把草的成分之一,其结构如图所示.下列叙述不正确的是( )
 中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用.有机物M是中药狼把草的成分之一,其结构如图所示.下列叙述不正确的是( )
中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用.有机物M是中药狼把草的成分之一,其结构如图所示.下列叙述不正确的是( )| A. | M是芳香族化合物,它的分子式为C9H5O4Cl | |
| B. | 1mol M最多能与含2 mol Br2的溴水发生反应 | |
| C. | 1mol M分别与足量的NaOH溶液、Na2CO3溶液反应,消耗两种物质的物质的量分别为4mol、2mol | |
| D. | 在一定条件下能发生取代、加成、水解、氧化等反应 |