题目内容
16.A、B、C、D 四种元素的核电荷数均小于 18,A 元素原子核外只有 1 个电子;B 是地壳中含量最多的元素;B、C 可形成两种化合物 CB 和 CB2,C 的最高正价与最低负价绝对值相等,CB 有毒,CB2可用于灭火;D+具有与 Ne 原子相同的电子层结构.(1)试判断 A、B、C、D 四种元素的名称.
A氢,B氧,C碳,D钠.
(2)由 A、B、D 三种元素组成的化合物的电子式为
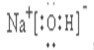 ,CB2的电子式为
,CB2的电子式为 .
.(3)D 和 B 组成的某种化合物为淡黄色固体,该物质的电子式为
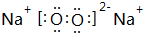 ,该物质与 CB2反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.
,该物质与 CB2反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.
分析 A、B、C、D四种元素的核电荷数均小于18,A元素原子核外只有1个电子,则A为H元素;B是地壳中含量最多的元素,则B为O元素;B、C可形成两种化合物CB和CB2,C的最高正价与最低负价绝对值相等,CB有毒,CB2可用于灭火,则C为碳元素;D+具有与Ne原子相同的电子层结构,则D为Na,以此解答该题.
解答 解:A、B、C、D四种元素的核电荷数均小于18,A元素原子核外只有1个电子,则A为H元素;B是地壳中含量最多的元素,则B为O元素;B、C可形成两种化合物CB和CB2,C的最高正价与最低负价绝对值相等,CB有毒,CB2可用于灭火,则C为碳元素;D+具有与Ne原子相同的电子层结构,则D为Na,
(1)(1)由上述分析可知,A为氢元素、B为氧元素、C为碳元素、D为钠元素,
故答案为:氢;氧;碳;钠;
(2)由A、B、D三种元素组成的化合物氢氧化钠是含有离子键和共价键的离子化合物,电子式为: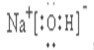 ,CB2为CO2,CO2的电子式为
,CB2为CO2,CO2的电子式为 ,
,
故答案为: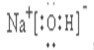 ;
; ;
;
(3)由B、D两种元素组成的Na2O2的电子式为 ,CO2与Na2O2反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2,
,CO2与Na2O2反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2,
故答案为: ;2Na2O2+2CO2=2Na2CO3+O2.
;2Na2O2+2CO2=2Na2CO3+O2.
点评 本题考查结构性质位置关系应用,为高频考点,侧重于学生的分析能力的考查,关键是推断元素,掌握电子式的书写,旨在考查学生对基础知识的巩固.

练习册系列答案
相关题目
16.下列说法正确的是 ( )
| A. | 在浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 | |
| B. | 葡萄糖注射液不产生丁达尔效应,不属于胶体 | |
| C. | 在Fe(0H)3胶体中.H+、K+、S2-、Br-能大量共存 | |
| D. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
7.化学与生活密切相关.下列生活中常见物质的俗名或名称与化学式相对应的是( )
| A. | 小苏打--Na2CO3 | B. | 烧碱--NaOH | C. | 铁红--Fe3O4 | D. | 明矾--KAl(SO4)2 |
4.下列叙述错误的是( )
| A. | SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同 | |
| B. | 制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中乙酸 | |
| C. | 用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 | |
| D. | 碳酸氢钠溶液中滴入苯酚的水溶液后不会放出二氧化碳 |
1.下列物质中,既能与强酸又能与强碱反应的是( )
①(NH4)2CO3 ②NaHCO3 ③Al2O3 ④Al(OH)3.
①(NH4)2CO3 ②NaHCO3 ③Al2O3 ④Al(OH)3.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
8.下列溶液中通入SO2一定不会产生沉淀的是( )
| A. | Ba(OH)2 | B. | Ba(NO3)2 | C. | BaC12 | D. | Na2S |
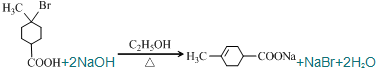
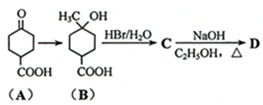 根据如图合成路线,请回答下列问题:
根据如图合成路线,请回答下列问题: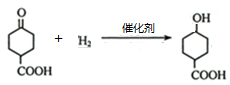 .
.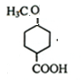 .
. .
.