题目内容
7.现有常见金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H.其中B是地壳中含量最多的金属.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).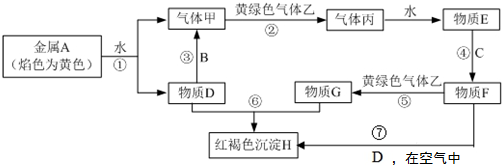
(1)写出化学式:BAl,GFeCl3
(2)写出离子反应方程式:
③2Al+2H2O+2OH-=2AlO2-+3H2↑
⑦4Fe2++8OH-+O2+2H2O=4Fe(OH)3.
分析 金属A焰色反应为黄色,故A为金属Na,乙是黄绿色气体,乙为Cl2,H为红褐色沉淀,为Fe(OH)3;由反应①Na→气体甲+D,考虑Na与水的反应,故甲为H2,D为NaOH,由NaOH+金属B→H2可知,B为金属Al,由甲+乙→丙,故丙为HCl,HCl溶于水的物质E,故E为盐酸;G+NaOH→Fe(OH)3,G含有Fe3+,由E(盐酸)$\stackrel{金属C}{→}$F$\stackrel{Cl_{2}}{→}$G可知,C为Fe,F为FeCl2,G为FeCl3,FeCl2与氢氧化钠在空气中生成氢氧化铁,符合各物质的转化关系,据此答题;
解答 解:金属A焰色反应为黄色,故A为金属Na,乙是黄绿色气体,乙为Cl2,H为红褐色沉淀,为Fe(OH)3;由反应①Na→气体甲+D,考虑Na与水的反应,故甲为H2,D为NaOH,由NaOH+金属B→H2可知,B为金属Al,由甲+乙→丙,故丙为HCl,HCl溶于水的物质E,故E为盐酸;G+NaOH→Fe(OH)3,G含有Fe3+,由E(盐酸)$\stackrel{金属C}{→}$F$\stackrel{Cl_{2}}{→}$G可知,C为Fe,F为FeCl2,G为FeCl3,FeCl2与氢氧化钠在空气中生成氢氧化铁,符合各物质的转化关系,
(1)根据上面的分析可知,B为Al,G为FeCl3,
故答案为:Al;FeCl3;
(2)反应③为铝与氢氧化钠反应生成偏铝酸钠和氢气,反应的离子反应方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑,反应⑦为FeCl2与氢氧化钠在空气中生成氢氧化铁,反应的离子反应方程式为4Fe2++8OH-+O2+2H2O=4Fe(OH)3,
故答案为:2Al+2H2O+2OH-=2AlO2-+3H2↑;4Fe2++8OH-+O2+2H2O=4Fe(OH)3;
点评 本题以无机框图题的形式考查Na、Al、Fe、Cl等元素单质及其化合物之间的相互转化关系、化学式的书写、离子方程式等,难度中等,注意基础知识的掌握.

| A. | 用蒸馏法可实现海水的淡化 | |
| B. | 乙醇可以用作“提取碘水中的碘”的萃取剂 | |
| C. | 用“蒸发结晶”的方法从氯化钠溶液中分离得到氯化钠晶体 | |
| D. | 除去氧化铁中的氧化铝杂质:用NaOH溶液浸泡,再过滤、洗涤、干燥,即可得到纯净氧化铁 |
①A2++B═B2++A ②A2++C═C2++A
③B2++C═C2++B ④C2++D═D2++C( )
| A. | 氧化性:A2+>B2+>C2+>D2+ | B. | 氧化性:D2+>C2+>B2+>A2+ | ||
| C. | 还原性:A>B>C>D | D. | 还原性:C>D>B>A |
| A. | 平衡逆向移动 | B. | 混合气体颜色比原来深 | ||
| C. | 混合气体颜色比原来浅 | D. | 混合气体的平均相对分子质量变小 |
| A. | 钠在氧气中燃烧,火焰呈黄色,产生白色固体 | |
| B. | 屠呦呦女士利用乙醇萃取青蒿汁中的青蒿素,获得了2015年度诺贝尔生理学或医学奖,为人类防治疟疾作出了重大贡献 | |
| C. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 | |
| D. | 钠投入水中,将沉在水底并熔化成小球,且有气泡产生 |
| A. | 物质在不电离的条件下,也能导电 | |
| B. | 若化学平衡向逆反应方向移动,则正反应速率不一定减小 | |
| C. | 硫酸钡、醋酸铵、碳酸氢钠都是强电解质 | |
| D. | 导电性强的溶液里自由移动离子数目一定比导电性弱的溶液里自由移动离子数目多 |