题目内容
11.(1)已知硫酸溶液的浓度越大密度也越大.40%的H2SO4溶液和50%的H2SO4溶液等质量混合后,得溶液溶质的质量分数等于(填“大于”“小于”或“等于”)45%;如果是等体积混合,混合以后所得溶液溶质的质量分数大于 (填“大于”“小于”或“等于”)45%(2)已知98%的浓H2SO4的物质的量浓度为18.4mol/L,试判断49%的H2SO4溶液的物质的量浓度
小于(填“大于”“小于”或“等于”)9.2mol/L.
(3)用(2)中98%的浓硫酸配制100mL浓度为1mol/L的稀硫酸.
①需要使用的主要仪器有量筒、烧杯、玻璃棒、100ml容量瓶、胶头滴管
②其操作步骤可分解为以下几步,请依次完成下述步骤中的空白处
A.用量筒量取5.4mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌
B.用约30mL蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都倒入容量瓶里
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里
D.检查100mL容量瓶,是否漏水
E.将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm用胶头滴管向容量瓶里
逐滴加入蒸馏水,到液面最低点恰好与刻线相切
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液
③正确的操作顺序是(用字母填写):D→A→C→B→E→G→F
④进行A步操作时,选用量筒的规格是A
A.10mL B.50mL C.100mL D.1000mL
⑤如果对装有浓硫酸的量筒仰视读数,配制的稀硫酸浓度将偏高(填“偏高”、“偏低”、“无影响”)
⑥A步骤操作完成时,必须冷却到室温后,才能进行后面的操作.
分析 (1)根据溶液的质量分数和质量计算混合后的溶质的质量分数,根据密度和体积计算溶液的总质量,根据硫酸的浓度越大,密度越大,判断质量分数关系;
(2)根据c=$\frac{1000ρω}{M}$计算,注意硫酸的浓度越大,密度越大,以此判断浓度大小关系;
(3)①根据配制一定物质的量浓度溶液的操作步骤选取实验仪器;
②A.根据溶液稀释前后溶质的物质的量不变计算所需浓硫酸溶液的体积;
E.依据定容的正确操作解答;
③配制一定物质的量浓度溶液的一般步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,据此排序;
④依据需要浓硫酸的体积选择合适量筒;
⑤如果对装有浓硫酸的量筒仰视读数,导致量取的浓硫酸体积偏大,硫酸的物质的量偏大,依据C
=$\frac{n}{V}$进行误差分析;
⑥容量瓶体积在标定的温度下才准确,结合浓硫酸稀释产生大量的热解答.
解答 解:(1)设原硫酸m,40%的H2SO4溶质为质量0.4m,50%的H2SO4溶质的质量为0.5m;混合后体积发生变化但质量不变,所以w(H2SO4)=$\frac{(0.4+0.5)m}{2m}$=45%,
如果等体积混合,设体积分别为Vml,40%的H2SO4溶液密度为ρ1,50%的H2SO4溶液密度为ρ2,则混合后溶液的质量分数为w(H2SO4)=$\frac{V•ρ1×40%+V•ρ2×50%}{V•ρ1+V•ρ2}$,
因硫酸的浓度越大,密度越大,则ρ1<ρ2,
则w(H2SO4)=$\frac{V•ρ1×40%+V•ρ2×50%}{V•ρ1+V•ρ2}$=(0.5-$\frac{0.1ρ1}{ρ1+ρ2}$)×100%>45%,
故答案为:等于;大于;
(2)根据c=$\frac{1000ρw}{M}$计算,设98%的浓H2SO4的密度为x,49%的H2SO4溶液的密度为y,物质的量浓度为c,
则:$\frac{1000x×98%}{98}$=18.4,$\frac{1000y×49%}{V}$=c
所以:$\frac{2x}{y}$,因硫酸的浓度越大,密度越大,则x>y,
则:c<9.2mol/L,
故答案为:小于;
(3)①配制一定物质的量浓度硫酸溶液的一般步骤有:量取、稀释、移液、洗涤、定容、摇匀等操作,一般用量筒量取浓硫酸溶液在烧杯中稀释,冷却后转移到100mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有玻璃棒、量筒、胶头滴管、小烧杯、100ml容量瓶,所以还缺少的仪器:100mL容量瓶、胶头滴管;
故答案为:100ml容量瓶、胶头滴管;
②A.设需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:18.4mol/L×V=100mL×1mol/L,解得V=5.4mL;
故答案为:5.4;
E.定容的正确操作为:将蒸馏水直接加入容量瓶,至液面接近刻度线1-2cm用胶头滴管向容量瓶里
逐滴加入蒸馏水,到液面最低点恰好与刻线相切;
故答案为:1-2cm;
③配制一定物质的量浓度溶液的一般步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,所以正确的操作顺序为:( D )→( A )→( C )→( B )→( E )→( G )→( F );
故答案为:( D )→( A )→( C )→( B )→( E )→( G )→( F );
④量取5.4mL浓硫酸,依据大而近的原则可知应选择10mL量筒;
故答案为:A;
⑤如果对装有浓硫酸的量筒仰视读数,导致量取的浓硫酸体积偏大,硫酸的物质的量偏大,依据C
=$\frac{n}{V}$可知溶液浓度偏高;
故答案为:偏高;
⑥浓硫酸稀释产生大量的热,未经冷却到室温就进行移液、洗涤、定容操作,导致溶液体积偏小,溶液浓度偏高,所以稀释后应冷却到室温后,再进行后面操作;
故答案为:冷却到室温.
点评 本题考查了溶液浓度的有关计算及一定物质的量浓度溶液的配制,明确硫酸浓度越大密度越大,熟悉配制一定物质的量浓度溶液的原理和操作步骤是解题关键,注意容量瓶使用方法和注意事项,题目难度中等.

 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案| A. | 除去镁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| B. | 用明矾净水是因为Al3+水解生成的胶状Al(OH)3具有很强的吸附性 | |
| C. | 在相同浓度的盐酸中,纯铁比含碳量较高的生铁反应速率快 | |
| D. | 冶金工业中可以利用铝热反应原理冶炼钒、铬、锰等金属 |
| A. | 该溶液中,Fe2+、NH4+、SO42-、S2-可以大量共存 | |
| B. | 该溶液中,H+、K+、NO3-、SO42-可以大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓硫酸,反应的离子方程式为:ClO2-+4H++3 Cl-=2Cl2↑+2 H2O |
| A. | 硅在自然界中既有游离态又有化合态 | |
| B. | 高温下SiO2能与Na2CO3固体反应生成Na2SiO3和CO2,说明硅酸酸性强于碳酸 | |
| C. | 因为玻璃中含有SiO2,所以不能用磨口玻璃塞的试剂瓶盛装碱性溶液 | |
| D. | SiO2能与氢氧化钠溶液和氢氟酸反应,所以SiO2是两性氧化物 |
 的名称是3,3,5,5-四甲基庚烷;
的名称是3,3,5,5-四甲基庚烷;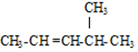 的名称是4-甲基-2-戊烯;
的名称是4-甲基-2-戊烯; ,则键线式为
,则键线式为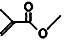 的物质的分子式为C5H8O2;
的物质的分子式为C5H8O2; 的一氯代物有5种;
的一氯代物有5种; -CH2-C≡CCH2-CH3,其中共平面的碳原子最多可能有15个.
-CH2-C≡CCH2-CH3,其中共平面的碳原子最多可能有15个.