题目内容
在下列各组溶液中,离子一定能大量共存的是( )
| A、含有0.1 mol?L-1H+的溶液中:NO3-、Na+、Cl-、Fe2+ |
| B、无色透明的溶液中:K+、Mg2+、Cl-、SO42- |
| C、强碱性溶液中:Na+、SO42-、HCO3-、K+ |
| D、能与铝反应生成H2的溶液中:Na+、Al3+、Cl-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.酸性条件下,NO3-具有强氧化性;
B.如离子之间不发生任何反应,则可大量共存;
C.HCO3-在碱性条件下不能大量存在;
D.能与铝反应生成H2的溶液可能呈强碱性,也可能为非氧化性酸溶液.
B.如离子之间不发生任何反应,则可大量共存;
C.HCO3-在碱性条件下不能大量存在;
D.能与铝反应生成H2的溶液可能呈强碱性,也可能为非氧化性酸溶液.
解答:
解:A.酸性条件下,NO3-具有强氧化性,Fe2+不能大量共存,故A错误;
B.离子之间不发生任何反应,可大量共存,故B正确;
C.HCO3-在碱性条件下不能大量存在,故C错误;
D.能与铝反应生成H2的溶液可能呈强碱性,也可能为非氧化性酸溶液,碱性条件下Al3+不能大量共存,故D错误.
故选B.
B.离子之间不发生任何反应,可大量共存,故B正确;
C.HCO3-在碱性条件下不能大量存在,故C错误;
D.能与铝反应生成H2的溶液可能呈强碱性,也可能为非氧化性酸溶液,碱性条件下Al3+不能大量共存,故D错误.
故选B.
点评:本题考查离子共存的正误判断,注意明确离子不能大量共存的一般情况以及题目所隐含的条件,为高频考点,属于中等难度的试题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关生产生活涉及的操作和原理说法正确的是( )
| A、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B、铁钉镀锌,将锌与电源负极相连,电镀过程需要控制电流强度、溶液pH等条件 |
| C、海轮外壳绑上锌板是采用牺牲阳极的阴极保护法,从而减缓钢铁腐蚀速率 |
| D、电解精炼铜时,阳极溶解铜的总质量和阴极析出铜的总质量相等 |
 已知常温时CH3COOH的电离平衡常数为Ka.该温度下向20mL 0.1mol?L-1CH3COOH溶液中逐滴加入0.1mol?L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )
已知常温时CH3COOH的电离平衡常数为Ka.该温度下向20mL 0.1mol?L-1CH3COOH溶液中逐滴加入0.1mol?L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )| A、a点表示的溶液中c(CH3COO-)+c(OH-)=10-3mol?L-1 | ||
| B、b点所示的溶液中c(CH3COO-)+c(OH-)>(CH3COOH)+c(H+) | ||
| C、c点的含义为:CH3COOH和NaOH恰好反应完全 | ||
D、a、b、c、d点表示的溶液中
|
今有下列仪器:铁架台、铁圈、铁夹、三脚架、石棉网、烧杯、漏斗、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、蒸馏烧瓶、坩埚钳、火柴、滤纸,从缺乏必要的仪器和用品的角度考虑,不能进行的分离操作是( )
| A、蒸发 | B、萃取 | C、过滤 | D、蒸馏 |
某化合物的结构(键线式)及球棍模型如图1:该有机分子的核磁共振氢谱图如图2(单位是ppm):下列关于该有机物的叙述正确的是( )
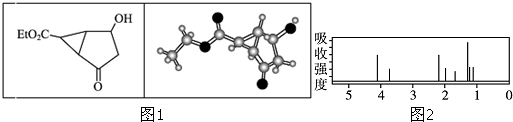

| A、该有机物不同化学环境的氢原子有6种 |
| B、该有机物属于芳香化合物 |
| C、键线式中的Et代表的基团为-CH3 |
| D、该有机物在一定条件下能够发生消去反应 |
下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)=c(NH4+) |
| B、两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1<10c2 |
| C、室温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液呈酸性 |
D、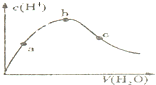 向冰醋酸中逐渐加水,有如图变化.a、b、c三点中水的电离程度最大的是b点 |
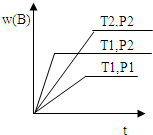 已知某反应aA(g)+bB(g)?cC(g)△H=Q 在密闭容器中进行,在不同温度(T1和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )
已知某反应aA(g)+bB(g)?cC(g)△H=Q 在密闭容器中进行,在不同温度(T1和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )| A、T1<T2,P1<P2,a+b>c,Q>0 |
| B、T1>T2,P1<P2,a+b<c,Q<0 |
| C、T1<T2,P1>P2,a+b<c,Q>0 |
| D、T1<T2,P1>P2,a+b>c,Q<0 |
汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,其反应原理是:2NO(g)+2CO(g)═N2(g)+2CO2(g),在298K、101kPa下△H=-113kJ?mol-1,△S=-145J?mol-1?K-1.下列说法中不正确的是( )
| A、该反应中反应物总能量高于生成物的总能量 |
| B、该反应只能在较高温度下才能自发进行 |
| C、该反应在较低温度下能自发进行,高温和催化剂条件只是加快反应的速率 |
| D、汽车尾气中的这两种气体会与人体血红蛋白结合而使人中毒 |