题目内容
下列判断中一定正确的是:
A.等物质的量的CaCl2及CaO2固体中阴、阳离子数之比均为2∶1
B.等质量的O2与O3中,氧原子的个数比为3∶2
C.分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1∶2
D.10mL 0.3mol·L-1NaCl与30mL0.1mol·L-1AlCl3溶液中Cl-物质的量浓度比为1∶3
C
【解析】
试题分析:A、CaCl2中的阴离子是氯离子,阳离子是钙离子,个数比是2:1,而CaO2中的阴离子是O22-,阳离子是钙离子,个数比是1:1,错误;B、等质量的O2与O3中O原子数目相等,所以个数比是1:1,错误;C、过氧化氢制取氧气时,O元素的化合价由-1价升高为0价,若生成1mol氧气,则转移电子的物质的量是2mol,而高锰酸钾制取氧气时,O元素的化合价由-2价升高为0价,若生成1mol氧气,转移电子的物质的量是4mol,所以当制得等质量O2时,转移电子数之比为2:4=1∶2,制取;D、0.3mol·L-1NaCl溶液中氯离子的浓度是0.3mol/L, 30mL0.1mol·L-1AlCl3溶液中氯离子的浓度也是0.3mol/L,所以二者的氯离子的浓度相等,错误,答案选C。
考点:考查溶液的浓度与离子浓度的关系,氧化还原反应的计算

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案
相关题目
下列反应中乙醇分子只断裂C-O键的是( )
| A、乙醇与金属钠反应产生氢气 | B、乙醇在浓硫酸存在下加热产生乙烯 | C、乙醇与氢卤酸发生取代反应生成卤代烃 | D、乙醇与酸性重铬酸钾溶液作用 |
下列实验操作与预期的实验目的或结论均正确的是 ( )
选项 | 实验操作 | 预期的实验目的或结论 |
A | 对某白色固体进行焰色反应实验,火焰呈黄色 | 该物质为钠盐 |
B | SO2通入某红色溶液中,溶液褪色 | 该溶液为品红溶液 |
C | pH均为12的NaOH溶液、氨水分别用蒸馏水稀释 m倍、n倍后的pH相同 | m<n |
D | 蔗糖溶液中加入少量稀硫酸加热,然后加银氨溶液再加热 | 验证蔗糖是否发生水解 |
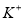 、
、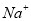 、
、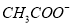 、Br-
、Br- 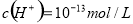 的溶液:
的溶液: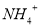 、
、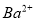 、
、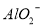 、
、