题目内容
(1)在一定温度和压强下,5体积气体A2跟15体积的气体B2完全化合生成10体积某气体C,则该气体C的化学式为(用A、B表示) .
(2)4gNaOH固体溶解后配制成100mL溶液,其物质的量浓度为 ,取出10mL该溶液,它的物质的量浓度为 ,将取出的10mL加水稀释至100mL,其物质的量浓度变为 .
(3)
S2-微粒中的中子数是 ,核外电子数是 .标准状况下11.2L的34SO2气体的质量是 .
(2)4gNaOH固体溶解后配制成100mL溶液,其物质的量浓度为
(3)
34 16 |
考点:阿伏加德罗定律及推论,物质的量的相关计算,化学方程式的有关计算,质量数与质子数、中子数之间的相互关系
专题:计算题,原子组成与结构专题
分析:(1)相同条件下,体积之比等于物质的量之比等于分子数之比,据此判断反应方程式各物质的化学计量数,根据方程式原子守恒计算C的化学式;
(2)n(NaOH)=
=0.1mol,结合c=
计算,注意溶液稀释前后溶质的物质的量不变;
(3)原子符号ZAX,左下角Z代表质子数,左上角A代表质量数,X代表元素符合,质量数=质子数+中子数,据此计算中子数,等于阴离子核外电子数=质子数+所带电荷数,根据n=
计算二氧化硫的物质的量,再根据m=nM计算二氧化硫的质量.
(2)n(NaOH)=
| 4g |
| 40g/mol |
| n |
| V |
(3)原子符号ZAX,左下角Z代表质子数,左上角A代表质量数,X代表元素符合,质量数=质子数+中子数,据此计算中子数,等于阴离子核外电子数=质子数+所带电荷数,根据n=
| V |
| Vm |
解答:
解:(1)由于5体积气体A2跟15体积的气体B2完全化合生成10体积某气体C,所以A2、B2、C的化学计量数之比为1:3:2,所以方程式为A2+3B2=2C,根据原子守恒可知C的化学式为AB3或B3A,故答案为:AB3或B3A;
(2)4gNaOH的物质的量为
=0.1mol,故氢氧化钠溶液的浓度为
=1mol/L,溶液是均匀的,取出10mL该溶液,与原氢氧化钠溶液的浓度相同为1mol/L,根据稀释定律,稀释前后溶质氢氧化钠的物质的量不变,令稀释后氢氧化钠溶液的浓度为c,则:10mL×1mol/L=100mL×c,解得c=0.1mol/L,
故答案为:1mol/L;1mol/L;0.1mol/L;
(3)
S2-微粒中的质子数为16,质量数为34,故中子数=34-16=18,核外电子数为16+2=18,11.2L的34SO2气体的物质的量为
=0.5mol,故该二氧化硫的质量为0.5mol×66g/mol=33g,
故答案为:18;18;33g.
(2)4gNaOH的物质的量为
| 4g |
| 40g/mol |
| 0.1mol |
| 0.1L |
故答案为:1mol/L;1mol/L;0.1mol/L;
(3)
34 16 |
| 11.2L |
| 22.4L/mol |
故答案为:18;18;33g.
点评:本题考查了核素中各微粒间的关系,物质的量的计算,涉及阿伏伽德罗定律及推论,难度不大,注意相关计算公式的运用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
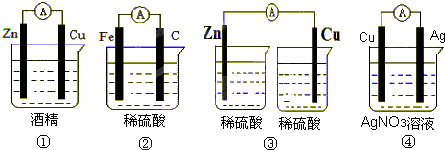
在电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
| A、将盐酸逐滴加入食盐溶液 |
| B、将硫酸逐滴加入氢氧化钡溶液 |
| C、将硫酸逐滴加入氢氧化钠溶液 |
| D、将醋酸逐滴加入氨水(NH3?H2O为弱电解质,CH3COONH4为强电解质) |