题目内容
下列有关用语表示正确的是( )
| A、漂白粉有效成分的化学式:CaCl2 | ||
B、Na+的结构示意图: | ||
C、原子核内有18个中子的氯原子:
| ||
| D、NH3?H2O的电离方程式:NH3?H2O═NH4++OH- |
考点:原子结构示意图,核素,分子式,电离方程式的书写
专题:化学用语专题
分析:A.漂白粉有效成分是次氯酸钙;
B.钠离子质子数为11,核外电子数为10;
C.氯原子质子数为17,质量数=质子数+中子数=17+18=35;
D.NH3?H2O是弱电解质,存在电离平衡.
B.钠离子质子数为11,核外电子数为10;
C.氯原子质子数为17,质量数=质子数+中子数=17+18=35;
D.NH3?H2O是弱电解质,存在电离平衡.
解答:
解:A.漂白粉有效成分是次氯酸钙,化学式为:Ca(ClO)2,故A错误;
B.钠离子质子数为11,核外电子数为10,故结构示意图为: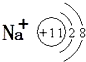 ,故B错误;
,故B错误;
C.氯原子质子数为17,质量数=质子数+中子数=17+18=35,故原子核内有18个中子的氯原子为:
Cl,故C正确;
D.NH3?H2O是弱电解质,电离方程式为:NH3?H2O?NH4++OH-,故D错误,
故选C.
B.钠离子质子数为11,核外电子数为10,故结构示意图为:
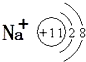 ,故B错误;
,故B错误;C.氯原子质子数为17,质量数=质子数+中子数=17+18=35,故原子核内有18个中子的氯原子为:
35 17 |
D.NH3?H2O是弱电解质,电离方程式为:NH3?H2O?NH4++OH-,故D错误,
故选C.
点评:本题考查漂白粉的组成、离子结构示意图的判断、原子符号的判断、电离方程式的判断等,难度不大.要注意弱电解质的电离方程式用可逆符号表示.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA表示阿伏加德罗常数的值.下列说法正确的是 ( )
| A、一定条件下,0.2mol SO2与足量O2充分反应,生成SO3分子数为0.2NA |
| B、0.1mol-NH2(氨基)中含有的电子数为0.7 NA |
| C、3.4克H2O2中含有的公用电子对数为0.1NA |
| D、常温常压下,16克O2和O3混合气体含有的氧原子数为NA |
只用一种试剂就可鉴别:C2H5OH、NaOH、C6H5OH、AgNO3、Na2CO3、KI六种透明溶液,这种试剂是( )
| A、稀盐酸 | B、氯化铁溶液 |
| C、溴水 | D、酸性高锰酸钾溶液 |
常用容量瓶的容积有( )
①50mL ②75mL ③100mL ④150mL ⑤200mL ⑥250mL ⑦500mL ⑧1000mL.
①50mL ②75mL ③100mL ④150mL ⑤200mL ⑥250mL ⑦500mL ⑧1000mL.
| A、①②⑥⑦ | B、②④⑦⑧ |
| C、①④⑥⑦ | D、③⑥⑦⑧ |
电化学原理在生产生活中应用广泛,下列叙述不正确的是( )
| A、在总反应为Zn+2H+=Zn2++H2的原电池中,正极材料为石墨,HN03做电解质溶液 |
B、 如图:若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 如图:若X为锌棒,开关K置于A或B处均可减缓铁的腐蚀 |
| C、电解饱和食盐水一段时间后,可通入HC1气体使溶液复原 |
| D、铂做电极,以KOH溶液为电解质溶液的甲烷-空气燃料电池,放电时的负极反应式:CH4+10OH--8e-=C032-+7H20 |
已知反应:①Cl2+2Kl═2KCl+I2②KClO3+6HCl═3Cl2↑+KCl+3H2O③2KIO3+Cl2═I2+2KClO3,下列说法正确的是( )
| A、上述三个反应都有单质生成,所以都是置换反应 |
| B、氧化性由强到弱顺序为KIO3>KClO3>Cl2>I2 |
| C、反应②中还原剂与氧化剂的物质的量之比为6:1 |
| D、③中1mol还原剂反应则氧化剂得到电子的物质的量为2mol |
化学与生活密切相关,下列生活中常见的名称与化学式相对应的是( )
| A、熟石灰-CaO |
| B、明矾-KAl(SO4)2 |
| C、铁红-Fe2O3 |
| D、硫酸铁-FeSO4 |
下列说法中正确的是( )
| A、一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物 |
| B、酸根离子中不可能含有金属元素 |
| C、酸性氧化物在一定条件下,都可以与碱反应生成盐和水 |
| D、还原产物只有还原性,氧化产物只有氧化性 |