题目内容
16.工业上利用氟碳铈矿(主要成分CeCO3F)提取CeCl3的一种工艺流程如图: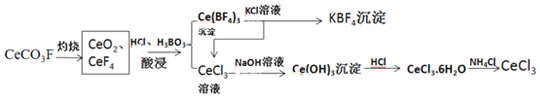
请回答下列问题:
(1)CeCO3F中,Ce元素的化合价为+3
(2)氟碳铈矿首先需要灼烧,实验室灼烧氟碳铈矿所需的实验仪器有bdef(填字母)
A.蒸发皿 b.泥三角 c.漏斗 d.酒精灯 e.三脚架 f.坩埚 g.烧杯 h.试管
(3)由CeCl3溶液得到CeCl3•6H2O晶体包含的实验步骤有洗涤、干燥、蒸发浓缩、冷却结晶
(4)酸浸过程中用稀硫酸和H2O2替换HCl不会造成环境污染.写出稀硫酸、H2O2与CeO2反应的离子方程式H2O2+2CeO2+6H+=2Ce3++4H2O+O2↑.
(5)向Ce(BF4)3中加入KCl溶液的目的是避免三价铈以Ce(BF4)3沉淀的形式损失或除去BF4-或提高CeCl3的产率.
(6)加热CeCl3•6H2O和NH4Cl的固体混合物可得到无水CeCl3,其中NH4Cl的作用是NH4Cl固体受热分解产生HCl,抑制CeCl3水解
(7)准确称取0.750gCeCl3样品置于锥形瓶中,加入适量过硫酸铵溶液将Ce3+氧化为Ce4+,然后用0.1000mol.l-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗25.00ml标准溶液.(已知:Fe2++Ce4+=Ce3++Fe3+)
①该样品中CeCl3的质量分数为82.2%(保留一位小数).
②若使用久置的(NH4)2Fe(SO4)2标准溶液进行滴定,测得该CeCl3样品的质量分数增大(填“偏大”、“偏小”或“无影响”)
分析 利用氟碳铈矿(主要成分CeCO3F)提取CeCl3的一种工艺流程为,CeCO3F焙烧得CeO2、CeF4,用盐酸和硼酸酸浸,过滤得沉淀Ce(BF)4和CeCl3滤液,Ce(BF)4与氯化钾溶液反应得到CeCl3和KBF,CeCl3与前面滤液中CeCl3的合并再加氢氧化钠,得Ce(OH)3沉淀,Ce(OH)3沉淀与盐酸反应可得CeCl3•6H2O,加热CeCl3•6H2O和NH4Cl的固体混合物可得到无水CeCl3,
(1)根据化合价代数和为0判断;
(2)灼烧需要泥三角、酒精灯、三脚架、坩埚;
(3)由CeCl3溶液得到CeCl3•6H2O晶体包含的实验步骤有蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
(4)在酸性条件下H2O2能还原CeO2生成Ce3+,根据元素守恒和电荷守恒书写离子方程式;
(5)向Ce(BF4)3中加入KCl溶液生成CeCl3和KBF,防止生成Ce(BF4)3沉淀;
(6)NH4Cl固体受热分解产生HCl,可以抑制CeCl3水解,据此答题;
(7)①0.1000mol•l-1(NH4)2Fe(SO4)2标准溶液体积25.00ml,含有亚铁离子的物质的量为2.5×10-3mol,根据反应Fe2++Ce4+═Ce3++Fe3+,利用Ce元素守恒可知,可计算出CeCl3的质量,进而确定样品中CeCl3的质量分数;
②若使用久置的(NH4)2Fe(SO4)2标准溶液进行滴定,由于亚铁离子被空气中氧气氧化,所以会消耗标准液的体积为偏大,据此分析.
解答 解:(1)根据化合价代数和为0可知,CeCO3F中,Ce元素的化合价为+3价,
故答案为:+3;
(2)灼烧需要泥三角、酒精灯、三脚架、坩埚;
故答案为:bdef;
(3)由CeCl3溶液得到CeCl3•6H2O晶体包含的实验步骤有蒸发浓缩、冷却结晶、过滤、洗涤、干燥,
故答案为:蒸发浓缩、冷却结晶;
(4)稀硫酸、H2O2与CeO2反应的离子方程式为:H2O2+2CeO2+6H+=2Ce3++4H2O+O2↑,
故答案为:H2O2+2CeO2+6H+=2Ce3++4H2O+O2↑;
(5)向Ce(BF4)3中加入KCl溶液生成CeCl3和KBF,这样做的目的是避免三价铈以Ce(BF4)3沉淀的形式损失或除去BF4-或提高CeCl3的产率,
故答案为:避免三价铈以Ce(BF4)3沉淀的形式损失或除去BF4-或提高CeCl3的产率;
(6)由于NH4Cl固体受热分解产生HCl,抑制CeCl3水解,所以加热CeCl3•6H2O和NH4Cl的固体混合物可得到无水CeCl3,
故答案为:NH4Cl固体受热分解产生HCl,抑制CeCl3水解;
(7)①0.1000mol•l-1(NH4)2Fe(SO4)2标准溶液体积25.00ml,含有亚铁离子的物质的量为2.5×10-3mol,根据反应Fe2++Ce4+═Ce3++Fe3+,利用Ce元素守恒可知,CeCl3的质量为2.5×10-3mol×246.5g/mol=0.6163g,所以样品中CeCl3的质量分数为$\frac{0.6163}{0.7500}$×100%=82.2%,
故答案为:82.2%;
②若使用久置的(NH4)2Fe(SO4)2标准溶液进行滴定,由于亚铁离子被空气中氧气氧化,所以会消耗标准液的体积为偏大,则测得该CeCl3样品的质量分数偏大,
故答案为:偏大.
点评 本题以提取CeCl3的一种工艺流程为载体,考查了化合价、离子反应、沉淀溶解平衡的计算、实验基本操作、化学计算等知识,侧重于考查学生的分析问题和解决问题的能量,注意相关基础知识的学习与积累,题目难度中等.

| A. | 胶体区别于其它分散系的本质特征是分散质的微粒直径在1nm~100nm | |
| B. | Fe(OH)3胶体带正电 | |
| C. | 往Fe(OH)3胶体中逐滴滴入硫酸溶液,现象是:先有红褐色沉淀后沉淀溶解 | |
| D. | Fe(OH)3胶体能够吸附水中悬浮的固体颗粒沉降,达到净水目的 |
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
| A. | 维生素C能促进人体对铁的吸收,利用了维生素C的氧化性 | |
| B. | 食品中大量添加苯甲酸钠灯防腐剂,可有效延长其保质期 | |
| C. | 《本草经集注》中记载了区别硝石(KNO3)和朴消(Na2SO4)的方法:“以火烧之,紫青烟起,乃真硝石也”,这是运用了焰色反应 | |
| D. | “从沙滩到用户”,计算机芯片的材料是指单质铁 |
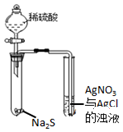
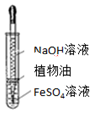
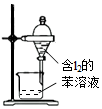
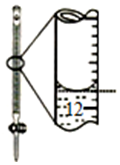
| A装置实验说明 Ksp(AgCl)>Ksp(Ag2S) | B.制备Fe(OH)2沉淀 | C.苯萃取碘水中的I2,分出水层后的操作 | D.记录滴定终点读数 为12.20mL |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
 奎宁酸和莽草酸是某些高等植物特有的脂环状有机 酸常共存在一起,其结构简式如图所示.下列说法正确的是( )
奎宁酸和莽草酸是某些高等植物特有的脂环状有机 酸常共存在一起,其结构简式如图所示.下列说法正确的是( )| A. | 奎宁酸与莽草酸互为同分异构体 | |
| B. | 两种酸含有的官能团完全相同 | |
| C. | 两种酸均能发生加成反应、聚合反应和取代反应 | |
| D. | 等物质的量的奎宁酸和莽草酸分别与足量Na反应,同温同压下产生H2的体积比为5:4 |
| A. | 加入过量浓盐酸:H+、Ba2+、Cl-、ClO- | |
| B. | 加入过量NaHCO3稀溶液:Na+、HCO3-、CO32-、C1O- | |
| C. | 加入过量 Fe(NO3)2溶液:Ba2+、NO3-、Fe2+、C1O- | |
| D. | 加入过量 Na2SO4溶液:Ba+、ClO-、Na+、SO42- |
| A. | 1 mol/L | B. | $\frac{100ρ}{103•65}$ mol/L | ||
| C. | $\frac{ρ}{103.65}$ mol/L | D. | $\frac{0.1ρ}{103•65}$ mol/L |