题目内容
5.常温下,用浓度为0.1000mol/L的盐酸分别逐滴加入到20.00mL 0.1000mol/L的两种一元碱MOH、ROH溶液中,PH随盐酸溶液体积的变化如图所示.下列说法正确的是( )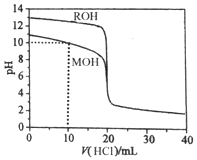
| A. | pH=10时,c(M+)>c(MOH)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 将上述MOH、ROH溶液等体积混合后,用盐酸滴定至MOH恰好反应时:c(R+)>c(M+)>c(H+)>c(OH-) | |
| C. | 10mL<V(HCl)<20mL时,c(M+)+c(MOH)<c(Cl-) | |
| D. | V(HCl)>20mL时,不可能存在:c(Cl-)>c(M+)=c(H+)>c(OH-) |
分析 根据图知,未加HCl溶液时,ROH的pH=13,说明c(OH-)=c(ROH),为强碱;MOH的pH小于13,则MOH为弱碱;
A.MOH溶液中加入10mLHCl溶液时,溶液中的溶质为等物质的量浓度的MOH和MCl,溶液呈碱性,说明MOH电离程度大于MCl水解程度,MOH电离程度较小;
B.将上述MOH、ROH溶液等体积混合后,用盐酸滴定至MOH恰好反应时,ROH已经完全反应,溶液中溶质为等物质的量浓度的MCl、RCl,MCl为强酸弱碱盐,M+水解导致溶液呈酸性,但水解程度较小;
C.10mL<V(HCl)<20mL时,溶液中溶质为MOH和MCl,且c(MCl)>c(MOH),溶液中存在物料守恒;
D.V(HCl)>20mL时,HCl过量导致溶液呈酸性,根据电荷守恒得c(Cl-)>c(M+),溶液中溶质存在有c(MCl)=c(HCl)、c(MCl)>c(HCl)或c(MCl)<c(HCl)三种情况.
解答 解:根据图知,未加HCl溶液时,ROH的pH=13,说明c(OH-)=c(ROH),为强碱;MOH的pH小于13,则MOH为弱碱;
A.MOH溶液中加入10mLHCl溶液时,溶液中的溶质为等物质的量浓度的MOH和MCl,溶液呈碱性,说明MOH电离程度大于MCl水解程度,MOH电离程度较小,氯离子不电离也不水解,所以c(MOH)<c(Cl-),故A错误;
B.将上述MOH、ROH溶液等体积混合后,用盐酸滴定至MOH恰好反应时,ROH已经完全反应,溶液中溶质为等物质的量浓度的MCl、RCl,MCl为强酸弱碱盐,M+水解导致溶液呈酸性,但水解程度较小,R+不水解,所以存在c(R+)>c(M+)>c(H+)>c(OH-),故B正确;
C.10mL<V(HCl)<20mL时,溶液中溶质为MOH和MCl,且c(MCl)>c(MOH),溶液中存在物料守恒c(M+)+c(MOH)>c(Cl-),故C错误;
D.V(HCl)>20mL时,HCl过量导致溶液呈酸性,根据电荷守恒得c(Cl-)>c(M+),溶液中溶质存在有c(MCl)=c(HCl)、c(MCl)>c(HCl)或c(MCl)<c(HCl)三种情况,可能出现c(Cl-)>c(M+)=c(H+)>c(OH-),故D错误;
故选B.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生分析、判断能力,明确各点溶液中溶质成分及其性质是解本题关键,易错选项是D,注意滴加过程中可能出现c(M+)>c(H+)、c(M+)=c(H+)、c(M+)<c(H+)情况,题目难度中等.

 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
| A. | CO是氧化剂 | B. | CO是还原剂 | ||
| C. | CO既是氧化剂又是还原剂 | D. | CO既不是氧化剂又不是还原剂 |
| ① | ② | ③ | ④ |
| 0.1mol/LNaOH溶液 | pH=11NaOH溶液 | 0.1mol/L CH3COOH溶液 | pH=3CH3COOH溶液 |
| A. | 由水电离出H+的浓度c(H+):①>③ | |
| B. | 将④加蒸馏水稀释至原来的100倍时,所得溶液的PH>5 | |
| C. | ①与③混合,若溶液pH=7,则体积:V(NaOH)>V(CH3COOH) | |
| D. | 等体积等PH的④溶液和盐酸分别与足量的Zn反应,④溶液生成同条件下氢气体积多 |
(1)配制待测液 将0.85g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成100mL溶液,所用的主要仪器有烧杯、玻璃棒、100mL容量瓶、量筒、胶头滴管.
(2)滴定 ①盛装0.20mol/L盐酸标准液应该用酸式滴定管.
②滴定时,应先向锥形瓶中加酚酞作为指示剂;滴定过程中两眼应该注视锥形瓶内溶液的颜色变化和滴定速度,滴定终点时,锥形瓶中的溶液的颜色变化是C.(填编号)
A.由黄色变为红色 B.由黄色变为橙色 C.由浅红色变为无色 D.由无色变为红色
③有关数据记录如表:
| 滴定序号 | 待测液体积(ml) | 所消耗盐酸标准液的体积(ml) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
(4)对几种假定情况的讨论:(填无影响、偏高、偏低)
①若用蒸馏水冲洗锥形瓶,则会使测定的结果无影响
②若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果偏高.
③若刚见到指示剂局部的颜色有变化就停止滴定,则会使测定结果偏低.
④读数时,若滴定前仰视,滴定后俯视,则会使测定结果偏低.
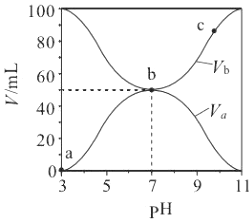
| A. | Ka(HA)的值与 Kb(BOH) 的值不相等 | |
| B. | b 点时,水电离出的 c(H+)=10-7mol/L | |
| C. | c 点时,c(A-)>c(B+) | |
| D. | a→c 过程中$\frac{c({A}^{-})}{c(O{H}^{-})•c(HA)}$不变 |
| 选项 | 实验 | 现象 | 结论 |
| A | 分别向2mL0.1mol/LNaHCO3,和2mL0.1mol/LNa2CO3溶液中滴加2mL 0.2mol/L的盐酸 | 盛有NaHCO3溶液试管产生气泡速度快 | 结合H+能力CO32->HCO3- |
| B | 将石蜡油(烷烃)蒸汽通过灼热的碎瓷片,并将产生的气体通人溴的四氯化碳溶液 | 溴的四氯化碳溶液褪色 | 生成气体中含有不饱和烃 |
| C | 向KI溶液中加入淀粉,然后滴入稀硫酸数滴 | 开始无明显现象,片刻溶液变蓝 | 氧化性:H2SO4>I2 |
| D | 向某溶液中加入盐酸 | 产生刺激性气味的气体和黄色沉淀 | 溶液中一定存在S2O32- |
| A. | A | B. | B | C. | C | D. | D |
| A. | 2-乙基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 2-甲基-1,3-丁二烯 | D. | 2,2-二甲基-3-戊炔 |