题目内容
已知90℃时,水的离子积常数为1×10-12.在此温度下,将pH=8NaOH溶液与pH=4的H2SO4溶液混合,也得到pH=7的混合溶液,则NaOH溶液与硫酸的体积比为 ;
若在0.10mol/L硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)= (Ksp[Cu(OH)2]=2.2×10-20).在0.1mol/L硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是 mol/L.
若在0.10mol/L硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=
考点:酸碱混合时的定性判断及有关ph的计算,pH的简单计算,难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:pH=8的Ba(OH)2溶液中氢氧根离子的物质的量浓度=
=10-4 mol/L,pH=4的H2SO4溶液中氢离子的物质的量浓度=10-4 mol/L,水的离子积常数Kw=10-12,即PH=6时,溶液呈中性,当混合溶液的pH=7时,溶液呈碱性,即Ba(OH)2过量,据此列式计算出NaOH溶液与硫酸的体积比;
根据溶度积常数及溶液中氢氧根离子浓度计算出c(Cu2+);
在0.1mol/L硫酸铜溶液中通入过量H2S气体,硫酸根离子浓度为0.1mol/L,根据溶液的电中性计算H+浓度.
| 10-12 |
| 10-8 |
根据溶度积常数及溶液中氢氧根离子浓度计算出c(Cu2+);
在0.1mol/L硫酸铜溶液中通入过量H2S气体,硫酸根离子浓度为0.1mol/L,根据溶液的电中性计算H+浓度.
解答:
解:当混合溶液的pH=7时,混合溶液中氢氧根离子的物质的量浓度=
=10-5 mol/L,
pH=8的Ba(OH)2溶液中氢氧根离子的物质的量浓度=
=10-4 mol/L,
pH=4的H2SO4溶液中氢离子的物质的量浓度=10-4 mol/L,
设硫酸的体积为x,Ba(OH)2溶液的体积为y,混合后pH=7,呈碱性,
则两种溶液混合后氢氧根离子的物质的量浓度列等式:
=10-5,解得:x:y=9:11;
根据题给Cu(OH)2的溶度积即可确定pH=8时,c(OH-)=10-6mol/L,Ksp[Cu(OH)2]=2.2×10-20,则:c(Cu2+)=
=2.2×10-8mol?L-1;
在0.1mol?L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的溶质为硫酸,c(SO42-)不变,为0.1mol?L-1,由电荷守恒可知c(H+)为0.2mol?L-1,
故答案为:9:11;2.2×10-8;0.2.
| 10-12 |
| 10-7 |
pH=8的Ba(OH)2溶液中氢氧根离子的物质的量浓度=
| 10-12 |
| 10-8 |
pH=4的H2SO4溶液中氢离子的物质的量浓度=10-4 mol/L,
设硫酸的体积为x,Ba(OH)2溶液的体积为y,混合后pH=7,呈碱性,
则两种溶液混合后氢氧根离子的物质的量浓度列等式:
| 10-4y-10-4x |
| x+y |
根据题给Cu(OH)2的溶度积即可确定pH=8时,c(OH-)=10-6mol/L,Ksp[Cu(OH)2]=2.2×10-20,则:c(Cu2+)=
| 2.2×10-20 |
| (1×10-6)2 |
在0.1mol?L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的溶质为硫酸,c(SO42-)不变,为0.1mol?L-1,由电荷守恒可知c(H+)为0.2mol?L-1,
故答案为:9:11;2.2×10-8;0.2.
点评:本题考查了酸碱反应的定性判断、难溶物的溶解平衡及其计算等知识,题目难度中等,注意掌握溶液酸碱性与溶液pH的计算方法,明确难溶物的溶解平衡及应用方法,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
NH3、H2O等是极性分子,CO2、BF3、CCl4等是极性键构成的非极性分子.根据上述事实可推出ABn型分子是非极性分子的经验规律是( )
| A、在ABn分子中A原子的所有价电子都参与成键 |
| B、在ABn分子中A的相对原子质量应小于B的相对原子质量 |
| C、在ABn分子中每个共价键的键长都相等 |
| D、分子中不能含有H原子 |
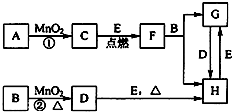 如图中所涉及的物质均为中学化学中的常见物质,其中C为单质,且为空气的主要成分之一;D为黄绿色气体;E为日常生活中应用最广泛的金属单质之一,其余为化合物.它们存在如图所示的转化关系,反应中生成的次要产物均已略去.
如图中所涉及的物质均为中学化学中的常见物质,其中C为单质,且为空气的主要成分之一;D为黄绿色气体;E为日常生活中应用最广泛的金属单质之一,其余为化合物.它们存在如图所示的转化关系,反应中生成的次要产物均已略去.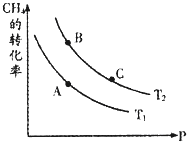 生产甲醇的原料CO、H2可由下列反应制取:CH4(g)+H2O(g)?CO(g)+3H2(g),试回答下列问题.
生产甲醇的原料CO、H2可由下列反应制取:CH4(g)+H2O(g)?CO(g)+3H2(g),试回答下列问题.