题目内容
在标准状况下,2.24L氢气与2L氧气反应生成 mL水.
考点:化学方程式的有关计算,气体摩尔体积
专题:计算题
分析:发生反应:2H2+O2
2H2O,氢气与氧气按物质的量之比2:1反应,实际氢气与氧气物质的量之比为2.24L:2L=1.12:1,故氢气不足,根据氢气计算生成水的质量,再根据V=
计算是的体积.
| ||
| m |
| ρ |
解答:
解:发生反应:2H2+O2
2H2O,氢气与氧气按物质的量之比2:1反应,实际氢气与氧气物质的量之比为2.24L:2L=1.12:1,故氢气不足,
氢气的物质的量=
=0.1mol,由方程式可知n(H2O)=n(H2)=0.1mol,故m(H2O)=0.1mol×18g/mol=1.8g,故生成水的体积=
=1.8mL,
故答案为:1.8.
| ||
氢气的物质的量=
| 2.24L |
| 22.4L/mol |
| 1.8g |
| 1g/mL |
故答案为:1.8.
点评:本题考查化学方程式计算,涉及过量计算,注意水不是气体,应先计算其质量,再结合密度计算水的体积.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案
相关题目
已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是( )
| A、16 g |
| B、32 g |
| C、64 g/mol |
| D、32 g/mol |
在水溶液中能大量共存的一组离子或离子分子组是( )
| A、I2、SO32-、Cl-、Na+ |
| B、K+、Cu2+、OH-、NO3- |
| C、NH4+、Na+、Br-、SO42- |
| D、Ag+、NH3*H2O、NO3-、Na+ |
A、B两元素可形成AB型离子化合物,且阴、阳离子具有相同的电子数.A、B的单质均能与水发生剧烈反应,反应中A单质做还原剂,B单质做氧化剂,则下列表述正确的是( )
| A、B元素原子的电子排布式为1S22S22P63S23P5 |
B、化合物AB的电子式为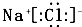 |
C、化合物AB的电子式为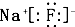 |
| D、A与水反应的离子方程式为Na+H2O═OH-+Na++H2 |
根据化学反应的实质是旧键断裂生成这一观点,下列变化不属于化学反应的是( )
| A、石墨转化为金刚石 |
| B、NaOH溶液与盐酸反应生成NaCl和H2O |
| C、NaCl熔化 |
| D、Na2O溶于水 |