题目内容
下列实验过程中产生的变化与对应的图形相符合的是( )
A、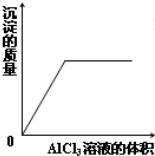 AlCl3溶液滴入NaOH溶液中 |
B、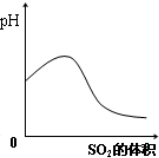 SO2气体通入氢硫酸中 |
C、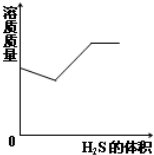 H2S气体通入NaOH溶液中 |
D、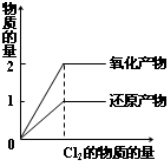 在一定量的H2S水溶液中逐渐通入Cl2 |
考点:镁、铝的重要化合物,氯气的化学性质,二氧化硫的化学性质
专题:图示题
分析:A.向NaOH溶液中滴加AlCl3溶液至过量,先发生反应:Al3++4OH-=AlO2-+2H2O,没有沉淀生成,后发生反应:3AlO2-+Al3++6H2O=4Al(OH)3↓有沉淀生成,再加AlCl3溶液振荡后不再消失;现象为:先没有沉淀,后生成沉淀,且所用氯化铝体积比为3:1,
B.SO2通入氢硫酸中发生反应生成S和水,溶液pH增大,SO2溶于水并和水反应生成亚硫酸,溶液pH增大减小;
C.H2S通入NaOH溶液中,反应生成Na2S,溶液质量先增大,然后Na2S再和H2S、H2O反应生成NaHS,溶液质量继续逐渐增大,最后不变;
D.在一定量的H2S水溶液中逐渐通入Cl2,先发生氧化还原反应:H2S+Cl2=2HCl+S↓,氧化产物S和还原产物HCl之比为1:2.
B.SO2通入氢硫酸中发生反应生成S和水,溶液pH增大,SO2溶于水并和水反应生成亚硫酸,溶液pH增大减小;
C.H2S通入NaOH溶液中,反应生成Na2S,溶液质量先增大,然后Na2S再和H2S、H2O反应生成NaHS,溶液质量继续逐渐增大,最后不变;
D.在一定量的H2S水溶液中逐渐通入Cl2,先发生氧化还原反应:H2S+Cl2=2HCl+S↓,氧化产物S和还原产物HCl之比为1:2.
解答:
A.向NaOH溶液中滴加AlCl3溶液至过量,先发生反应:Al3++4OH-=AlO2-+2H2O,没有沉淀生成,后发生反应:3AlO2-+Al3++6H2O=4Al(OH)3↓有沉淀生成,再加AlCl3溶液振荡后不再消失;现象为:先没有沉淀,后生成沉淀,且所用氯化铝体积比为3:1;故A错误;
B.SO2气体通入氢硫酸中,发生的反应为:2H2S+SO2═3S↓+2H2O,氢硫酸的量开始减少,所以酸性减弱,PH值变大,当硫化氢消耗完毕时,SO2溶于水并和水反应生成亚硫酸,溶液的酸性增强,PH值变小,故B正确;
C、H2S气体通入NaOH溶液中,开始发生反应的方程式为:H2S+2NaOH=Na2S+2H2O,溶液质量逐渐增大,当全部生成Na2S后,继续通入硫化氢生成硫氢化钠,发生反应:Na2S+2H2O+H2S=2NaHS,溶液质量继续逐渐增大,当Na2S消耗完毕时,溶液质量不再改变,故C错误;
D.在一定量的H2S水溶液中逐渐通入Cl2,先发生氧化还原反应:H2S+Cl2=2HCl+S↓,Cl2为氧化剂,H2S为还原剂,HCl为还原产物,S为氧化产物,反应最后氧化产物和还原产物之比为1:2,故D错误;
故选B.
B.SO2气体通入氢硫酸中,发生的反应为:2H2S+SO2═3S↓+2H2O,氢硫酸的量开始减少,所以酸性减弱,PH值变大,当硫化氢消耗完毕时,SO2溶于水并和水反应生成亚硫酸,溶液的酸性增强,PH值变小,故B正确;
C、H2S气体通入NaOH溶液中,开始发生反应的方程式为:H2S+2NaOH=Na2S+2H2O,溶液质量逐渐增大,当全部生成Na2S后,继续通入硫化氢生成硫氢化钠,发生反应:Na2S+2H2O+H2S=2NaHS,溶液质量继续逐渐增大,当Na2S消耗完毕时,溶液质量不再改变,故C错误;
D.在一定量的H2S水溶液中逐渐通入Cl2,先发生氧化还原反应:H2S+Cl2=2HCl+S↓,Cl2为氧化剂,H2S为还原剂,HCl为还原产物,S为氧化产物,反应最后氧化产物和还原产物之比为1:2,故D错误;
故选B.
点评:本题考查了图象分析,明确物质的性质是解本题关键,知道物质之间的反应、溶液中离子浓度变化,分清氧化产物和还原产物即可解答,题目难度不大.

练习册系列答案
相关题目
足量的铜与浓硫酸反应,当反应停止后,加入下列物质后,铜又能继续溶解的是( )
①稀硫酸 ②氧化铁 ③铁 ④硝酸 ⑤硝酸钾.
①稀硫酸 ②氧化铁 ③铁 ④硝酸 ⑤硝酸钾.
| A、②④⑤ | B、①④⑤ |
| C、③④ | D、③④⑤ |
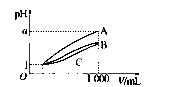 pH=1的三种酸溶液A、B、C各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )
pH=1的三种酸溶液A、B、C各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是( )| A、溶液的物质的量浓度C>B>A |
| B、酸性A>B>C |
| C、若a=4,则A是强酸,B、C是弱酸 |
| D、若1<a<4,则A、B、C都是弱酸 |
已知氧化性Fe3+>I2.FeI2溶液中通入一定量的Cl2,发生反应的离子方程式为:a Fe2++bI-+c Cl2→d Fe3++e I2+f Cl-下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
| A、2 4 3 2 2 6 |
| B、0 2 1 0 1 2 |
| C、2 0 1 2 0 2 |
| D、2 10 6 2 5 12 |
