题目内容
一定温度下,用水稀释0.1mol?L-1的一元弱酸HA,随着水量的增加,下列数值一定增大的是( )
| A、Kw |
| B、c(H+)/Ka |
| C、c(HA)/c(A-) |
| D、c(OH-) |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:加水稀释弱酸,促进弱酸电离,但氢离子浓度减小,温度不变水的离子积常数不变,则溶液中氢氧根离子浓度增大,据此分析解答.
解答:
解:A.温度不变,水的离子积常数不变,故A错误;
B.加水稀释促进弱酸电离,氢离子的物质的量增大,但溶液体积增大的倍数大于氢离子增大的物质的量,溶液氢原子浓度减小,温度不变,电离平衡常数不变,所以
减小,故B错误;
C.加水稀释促进弱酸电离,所以酸分子个数减小,酸根离子个数增大,则
,故C错误;
D.加水稀释,溶液中氢离子浓度减小,温度不变,水的离子积常数不变,则氢氧根离子浓度增大,故D正确.
故选D.
B.加水稀释促进弱酸电离,氢离子的物质的量增大,但溶液体积增大的倍数大于氢离子增大的物质的量,溶液氢原子浓度减小,温度不变,电离平衡常数不变,所以
| c(H +) |
| Ka |
C.加水稀释促进弱酸电离,所以酸分子个数减小,酸根离子个数增大,则
| c(HA) |
| c(A-) |
D.加水稀释,溶液中氢离子浓度减小,温度不变,水的离子积常数不变,则氢氧根离子浓度增大,故D正确.
故选D.
点评:本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,注意酸的电离平衡常数、水的离子积常数只与温度有关,与溶液的酸碱性无关,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
等质量的下列有机物完全燃烧,消耗O2最多的是( )
| A、CH4 |
| B、CH3CH3 |
| C、C2H2 |
| D、C3H8 |
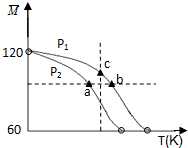 已知 (CH3COOH)2(g)?2CH3COOH (g),经实验测得不同压强下,体系的平均摩尔质量(
已知 (CH3COOH)2(g)?2CH3COOH (g),经实验测得不同压强下,体系的平均摩尔质量(. |
| M |
| m总 |
| n总 |
| A、该过程的△H<0 |
| B、气体压强:P(a)<P(b)=P(c) |
| C、平衡常数:K(a)=K(b)<K(c) |
| D、测定乙酸的相对分子质量要在高压、低温条件 |
有一种含氨和氯化铵物质的量相等的混合溶液,其pH为9.3,下列说法中错误的是( )
| A、氨水的电离作用大于氯化铵的水解作用 |
| B、氯化铵的水解作用大于氨水的电离作用 |
| C、氨水的存在抑制了氯化铵的水解 |
| D、氯化铵的存在抑制了氨水的电离 |
某金属与稀硝酸反应生成一种硝酸盐,该硝酸盐受热分解生成NO2、O2和一种固体,该固体中金属元素的化合价比原硝酸盐中该金属的化合价高,则该硝酸盐分解后生成的NO2和O2的物质的量之比为( )
| A、8:1 | B、4:1 |
| C、2:1 | D、1:1 |
下列说法正确的是( )
| A、铅蓄电池放电时的阳极和充电时的负极均发生氧化反应 |
| B、用饱和Na2CO3溶液处理BaSO4沉淀,可将BaSO4转化为BaCO3 |
| C、一定温度下,反应Mg(1)+Cl2(g)═MgCl2(1)的△H<0,△S<0 |
| D、pH=5的CH3COOH溶液和pH=5的NH4C1溶液中,水的电离程度相同 |
不能实现下列物质间直接转化的单质是( )
单
氧化物
酸或碱
盐.
单
| O2 |
| H2O |
| +NaOH或HCl |
| A、硫 | B、碳 | C、铜 | D、钙 |