题目内容
(1)写出下列官能团的名称:
①-COOH ②-OH
(2)现有4种有机物:①乙烯,②乙醇,③乙酸,④乙酸乙酯(填写结构简式):
能发生水解反应的是
具有酸性且能发生酯化反应的是 .
能发生加成反应的是 .
①-COOH
(2)现有4种有机物:①乙烯,②乙醇,③乙酸,④乙酸乙酯(填写结构简式):
能发生水解反应的是
具有酸性且能发生酯化反应的是
能发生加成反应的是
考点:烃的衍生物官能团,有机物分子中的官能团及其结构
专题:有机化学基础
分析:(1)决定有机物化学性质的原子或者原子团称为官能团,常见的官能团有:碳碳双键、碳碳三键、羟基、羧基、醛基、卤素原子、酯基等;据此进行解答;
(2)①乙烯含有C=C官能团,可发生加成反应;
②乙醇含有-OH官能团,可发生酯化、取代、消去反应;
③乙酸含有-COOH,具有酸性,可发生置换、取代反应;
④乙酸乙酯含有-COO-官能团,可发生水解反应.
(2)①乙烯含有C=C官能团,可发生加成反应;
②乙醇含有-OH官能团,可发生酯化、取代、消去反应;
③乙酸含有-COOH,具有酸性,可发生置换、取代反应;
④乙酸乙酯含有-COO-官能团,可发生水解反应.
解答:
解:(1)-COOH:为羧基,为羧酸的官能团;-OH:为醇类或酚类的官能团,名称为羟基;
故答案为:羧基;羟基;
(2)①能发生水解反应的是乙酸乙酯;
②具有酸性且能发生酯化反应的是乙酸;
③能发生加成反应的是乙烯,
故答案为:CH3COOCH2CH3;CH3COOH;CH2=CH2.
故答案为:羧基;羟基;
(2)①能发生水解反应的是乙酸乙酯;
②具有酸性且能发生酯化反应的是乙酸;
③能发生加成反应的是乙烯,
故答案为:CH3COOCH2CH3;CH3COOH;CH2=CH2.
点评:本题考查有机物的结构和性质,较基础,本题注意把握有机物的官能团的结构和性质,把握官能团,是学习有机化学的关键,学习中注意积累.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
在一密闭容器中盛有过量的NaHCO3和少量的Na2O2,将其加热到300℃经充分反应后,排出气体,容器内残留的固体是( )
| A、NaHCO3和NaOH |
| B、Na2CO3和NaOH |
| C、NaHCO3和Na2CO3 |
| D、Na2CO3 |
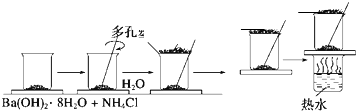 在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20g已研磨成粉末的Ba(OH)2?8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10g NH4Cl晶体,根据实验步骤,填写下表,并回答问题.
在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20g已研磨成粉末的Ba(OH)2?8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10g NH4Cl晶体,根据实验步骤,填写下表,并回答问题. 利用如图装置测定中和反应的反应热的实验步骤如下:
利用如图装置测定中和反应的反应热的实验步骤如下: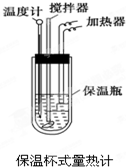 在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中(如图)将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.