题目内容
6.分枝酸可用于生化研究,其结构简式为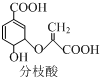 ,下列关于分枝酸的说法不正确的是( )
,下列关于分枝酸的说法不正确的是( )| A. | 分子中含有3种含氧官能团 | |
| B. | 1 mol分枝酸最多可与3mol NaOH发生中和反应 | |
| C. | 在一定条件下可与乙醇、乙酸反应,且反应类型相同 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,但褪色原理不同 |
分析 该有机物中含有碳碳双键、醇羟基、醚键、羧基,具有烯烃、酚、醚和羧酸性质,能发生加成反应、加聚反应、氧化反应、取代反应等,据此分析解答.
解答 解:A.该物质中含有碳碳双键、醇羟基、醚键和羧基四种官能团,但含有3种含氧官能团,故A正确;
B.不是苯环,只有-COOH与NaOH反应,则1mol分枝酸最多可与2molNaOH发生中和反应,故B错误;
C.含-COOH与乙醇发生酯化反应,含-OH与乙酸发生酯化反应,故C正确;
D.碳碳双键与溴的四氯化碳溶液发生加成反应,双键与-OH均能被酸性高锰酸钾溶液氧化,原理不同,故D正确;
故选B.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,注意该分子中没有酚羟基,为易错点.

练习册系列答案
相关题目
17.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | lmol•L?1的NaCl溶液中所含Na+为NA个 | |
| B. | 标准状况下,11.2 L SO3所含的分子数为0.5NA | |
| C. | 0.1 mol CH4所含的电子数为1NA | |
| D. | 2molNO和1mol O2混合,所得气体分子数为2NA |
1. 弱酸HA的电离常数Ka=$\frac{c({H}^{+})•c({A}^{-})}{c(HA)}$.25℃时,几种弱酸的电离常数如下:
弱酸HA的电离常数Ka=$\frac{c({H}^{+})•c({A}^{-})}{c(HA)}$.25℃时,几种弱酸的电离常数如下:
(1)根据上表数据填空:
①物质的量浓度相同的四种酸,其pH由大到小的顺序是HCN>H2CO3>CH3COOH>HNO2.
②分别向等体积、相同pH的HCl溶液和CH3COOH溶液中加入足量的Zn粉,反应刚开始时产生H2的速率:v(HCl)=v(CH3COOH)(填“=”、“>”或“<”下同),反应完全后,所得氢气的质量:m(H2)盐酸<m(H2)醋酸.
③将0.2 mol/L HCN溶液与0.1 mol/L Na2CO3溶液等体积混合,发生反应的化学方程式为HCN+Na2CO3═NaCN+NaHCO3.
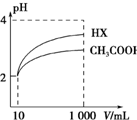
(2)体积均为10 mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000 mL,稀释过程中溶液pH变化如图所示.稀释后,HX溶液中水电离的c(H+) 比醋酸溶液中水电离的c(H+)大;电离常数Ka(HX>Ka(CH3COOH)(填“>”、“=”或“<”),理由是稀释相同倍数,较强的酸pH变化较大,较强的酸电离常数较大,从图中看出HX的pH变化较大.
 弱酸HA的电离常数Ka=$\frac{c({H}^{+})•c({A}^{-})}{c(HA)}$.25℃时,几种弱酸的电离常数如下:
弱酸HA的电离常数Ka=$\frac{c({H}^{+})•c({A}^{-})}{c(HA)}$.25℃时,几种弱酸的电离常数如下:| 弱酸化学式 | HNO2 | CH3COOH | HCN | H2CO3 |
| 电离常数 | 5.1×10-4 | 1.8×10-5 | 6.2×10-10 | K1=4.4×10-7 K2=4.7×10-11 |
①物质的量浓度相同的四种酸,其pH由大到小的顺序是HCN>H2CO3>CH3COOH>HNO2.
②分别向等体积、相同pH的HCl溶液和CH3COOH溶液中加入足量的Zn粉,反应刚开始时产生H2的速率:v(HCl)=v(CH3COOH)(填“=”、“>”或“<”下同),反应完全后,所得氢气的质量:m(H2)盐酸<m(H2)醋酸.
③将0.2 mol/L HCN溶液与0.1 mol/L Na2CO3溶液等体积混合,发生反应的化学方程式为HCN+Na2CO3═NaCN+NaHCO3.
(2)体积均为10 mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000 mL,稀释过程中溶液pH变化如图所示.稀释后,HX溶液中水电离的c(H+) 比醋酸溶液中水电离的c(H+)大;电离常数Ka(HX>Ka(CH3COOH)(填“>”、“=”或“<”),理由是稀释相同倍数,较强的酸pH变化较大,较强的酸电离常数较大,从图中看出HX的pH变化较大.
11.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,48gO3中所含的氧原子数为3NA | |
| B. | 1.8gNH4+中所含质子数为0.1NA | |
| C. | 标况下,11.2L氧气中所含原子数为0.5NA | |
| D. | 2.4g金属镁变成离子时得到的电子数为0.2NA |
18.下列物质中,不能电离出酸根离子的是( )
| A. | Na2CO3 | B. | KMnO4 | C. | KOH | D. | H2SO4 |
15.下列选项中,对于指定项目的数目前后相等的是( )
| A. | 电子数:17gOH-与1mol-OH | |
| B. | 双键数目:1mol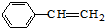 与4mol C2H4 与4mol C2H4 | |
| C. | 分子数:常温常压下16g氧气与4g氦气 | |
| D. | 阴离子总数:72gCaO2与62g Na2O |
16.单质铜及其化合物一般都具有特殊的颜色,如
某学校学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O,进行了认真的研究.
Ⅰ.查阅资料得出下列信息:
①Cu2O属于碱性氧化物; ②高温灼烧CuO生成Cu2O;
③Cu2O在酸性条件下能发生反应:Cu2O+2H+═Cu+Cu2++H2O.
Ⅱ.设计实验方案:
方案1:取该红色固体溶于足量的稀硝酸中,观察溶液颜色变化.
方案2:取该红色固体溶于足量的稀硫酸中,观察溶液是否呈蓝色.
方案3:称得干燥坩埚的质量为a g,取红色固体置于坩埚中称得总质量为b g,在空气中高温灼烧至质量恒定,称得最后总质量为c g.
(1)写出Cu2O与稀硝酸反应的化学方程式:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O.
(2)请你评价方案1和方案2的合理性,并简述理由:
方案1:不合理,因为铜和氧化亚铜均可溶于稀硝酸形成蓝色溶液.
方案2:合理,因为氧化亚铜与稀硫酸生成Cu和Cu2+,导致溶液呈蓝色.
(3)方案3中,若确认红色固体中含有Cu2O,则a、b、c的关系为c<$\frac{9b-a}{8}$,在该实验方案中最少应进行4次称量.
Ⅲ.学习小组乙设计了新的探究方案,拟根据干燥管中无水硫酸铜是否变蓝判断红色固体中是否含有Cu2O,装置如图所示.

(4)该探究方案中检验气体发生装置气密性的方法为:关闭活塞,从长颈漏斗向试管中注入一定量的水,使漏斗内液面高于试管内液面,静置后若漏斗内液面不下降,则装置的气密性良好;液面下降,则装置漏气;(说明操作方法、现象和结论).
(5)为确保探究的科学、合理和安全,你认为实验中还应采取的措施有ABC(填序号).
A.在氢气发生装置与硬质玻璃管之间增加一个干燥装置
B.加热前先排尽装置中的空气
C.在盛有无水硫酸铜的干燥管后再连接一个装有碱石灰的干燥管.
| Cu | Cu2O | CuO | Cu(OH)2 | CuSO4•5H2O |
| 红色(或紫红色) | 红色(或砖红色) | 黑色 | 蓝色 | 蓝色 |
Ⅰ.查阅资料得出下列信息:
①Cu2O属于碱性氧化物; ②高温灼烧CuO生成Cu2O;
③Cu2O在酸性条件下能发生反应:Cu2O+2H+═Cu+Cu2++H2O.
Ⅱ.设计实验方案:
方案1:取该红色固体溶于足量的稀硝酸中,观察溶液颜色变化.
方案2:取该红色固体溶于足量的稀硫酸中,观察溶液是否呈蓝色.
方案3:称得干燥坩埚的质量为a g,取红色固体置于坩埚中称得总质量为b g,在空气中高温灼烧至质量恒定,称得最后总质量为c g.
(1)写出Cu2O与稀硝酸反应的化学方程式:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O.
(2)请你评价方案1和方案2的合理性,并简述理由:
方案1:不合理,因为铜和氧化亚铜均可溶于稀硝酸形成蓝色溶液.
方案2:合理,因为氧化亚铜与稀硫酸生成Cu和Cu2+,导致溶液呈蓝色.
(3)方案3中,若确认红色固体中含有Cu2O,则a、b、c的关系为c<$\frac{9b-a}{8}$,在该实验方案中最少应进行4次称量.
Ⅲ.学习小组乙设计了新的探究方案,拟根据干燥管中无水硫酸铜是否变蓝判断红色固体中是否含有Cu2O,装置如图所示.

(4)该探究方案中检验气体发生装置气密性的方法为:关闭活塞,从长颈漏斗向试管中注入一定量的水,使漏斗内液面高于试管内液面,静置后若漏斗内液面不下降,则装置的气密性良好;液面下降,则装置漏气;(说明操作方法、现象和结论).
(5)为确保探究的科学、合理和安全,你认为实验中还应采取的措施有ABC(填序号).
A.在氢气发生装置与硬质玻璃管之间增加一个干燥装置
B.加热前先排尽装置中的空气
C.在盛有无水硫酸铜的干燥管后再连接一个装有碱石灰的干燥管.