题目内容
某实验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式。
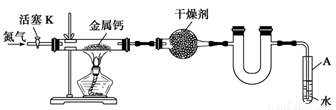
(1)反应过程中末端导管必须始终插入试管A的水中,目的是_____________________。
(2)制备氮化钙的操作步骤是:
①打开活塞K并通入N2;
②点燃酒精灯,进行反应;
③反应结束后,__________________________________________________________;
④拆除装置,取出产物。
(3)数据记录如下:(假设反应完全)
|
空硬质管质 量m0/g |
硬质管与钙的 质量m1/g |
硬质管与产物 的质量m2/g |
|
14.80 |
15.08 |
15.15 |
① 计算得到实验式CaxN2,其中x=________。
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:
______________________________________________________________________。
(1)防止空气中的氧气通过末端导管进入实验装置,氧化单质钙,生成氧化钙,引入杂质 (1分)
(2)熄灭酒精灯,待玻璃管冷却至室温,停止通入氮气,并关闭活塞 (2分)
(3)①2.80 (1分) ②x<3,产物中生成了CaO导致钙的质量分数减小 (2分)
【解析】
试题分析:(1)由于钙非常活泼需防止空气中的氧气通过末端导管进入实验装置通过末端导管进入实验装置,氧化单质钙,生成氧化钙,引入杂质
(2)由实验步骤可知应为熄灭酒精灯,待玻璃管冷却至室温,停止通入氮气,并关闭活塞
(3))m(Ca)=15.08-14.80=0.28g;m(N)=15.15-15.08=0.07g;则 =(
=(  )/(
)/( )解得X=2.80
)解得X=2.80
①2.80 ②若通入的N2中混有少量O2产物中生成了CaO导致钙的质量分数减小,所以x<3。
考点:考查实验基本操作、物质制备、计算等相关知识

 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。

发生的反应如下:

反应物和产物的相关数据列表如下:
|
|
沸点/℃ |
密度/g·cm-3 |
水中溶解性 |
|
正丁醇 |
117.2 |
0.8109 |
微溶 |
|
正丁醛 |
75.7 |
0.8017 |
微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95℃,在E中收集90℃以上的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由 。
(2)加入沸石的作用是 ,若加热后发现未加入沸石,应采取的正确方法是 。
(3)上述装置图中,B仪器的名称是 ,D仪器的名称是 。
(4)将正丁醛粗产品置于分液漏斗中分水时,水在 层(填“上”或“下”)。
(5)反应温度应保持在90~95℃,其原因是 。
(6)本实验中,正丁醛的产率为 %。


