题目内容
Ⅰ.某一反应体系中有反应物和生成物共八种物质:KMnO4、SO2、CuS、H2SO4、CuSO4、K2SO4 MnSO4、H2O.反应中氧化过程如下:CuS→SO2.写出并配平该反应的化学方程式
Ⅱ.如何降低大气中 CO2的含量及有效地开发利用碳资源是目前亟待解决的问题
(1)工业上一般以 CO 和 H2 为原料合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ?mol-1,下列措施中既有利于增大反应速率又有利于提高 CO 转化率的是
A.随时将 CH3OH 与反应混合物分离 B.降低反应温度 C.增大体系压强 D.使用高效催化剂
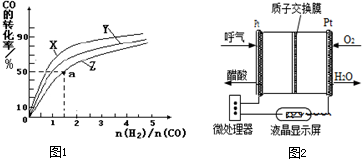
(2)在容积为 2L 的恒容容器中,分别研究在 230℃、250℃和 270℃三种温度下合成甲醇的规律.如图1是上述三种温度下不同的 H2和 CO 的起始组成比(起始时 CO 的物质的量均为 2mol)与 CO平衡转化率的关系.在上述三种温度中,曲线 Z 对应的温度是 ,a 点混合气体的平均分子量为 (小数点后保留两位数字)
(3)如图2所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,则该电池的负极反应式为 .
Ⅱ.如何降低大气中 CO2的含量及有效地开发利用碳资源是目前亟待解决的问题
(1)工业上一般以 CO 和 H2 为原料合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ?mol-1,下列措施中既有利于增大反应速率又有利于提高 CO 转化率的是
A.随时将 CH3OH 与反应混合物分离 B.降低反应温度 C.增大体系压强 D.使用高效催化剂
(2)在容积为 2L 的恒容容器中,分别研究在 230℃、250℃和 270℃三种温度下合成甲醇的规律.如图1是上述三种温度下不同的 H2和 CO 的起始组成比(起始时 CO 的物质的量均为 2mol)与 CO平衡转化率的关系.在上述三种温度中,曲线 Z 对应的温度是
(3)如图2所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,则该电池的负极反应式为

考点:化学平衡的影响因素,氧化还原反应方程式的配平,化学电源新型电池,转化率随温度、压强的变化曲线
专题:基本概念与基本理论
分析:I.该反应中氧化过程为CuS→SO2,CuS作还原剂,要使该反应发生,需要氧化剂,酸性条件下KMnO4具有强氧化性,所以可以作氧化剂,则MnSO4为还原产物,溶液呈酸性,硫酸是反应物,水是生成物,据此书写方程式;
II.(1)该可逆反应是反应前后气体体积减小的放热反应,增大反应速率又有利于提高CO转化率,应该增大压强;
(2)该反应的正反应是放热反应,升高温度平衡向逆反应方向移动,则CO的转化率降低,所以Z表示最高温度下的反应;
a点时,n(H2)/n(CO)=1.5,反应开始时n(CO)=2mol,则开始时n(H2)=3mol,CO的转化率为50%,平衡时n(CO)=2mol×(1-50%)=1mol,n(H2)=3mol-2×(2mol×50%)=2mol,n(CH3OH)=1mol,平衡时混合气体的物质的量=1mol+2mol+1mol=4mol,混合气体质量=2mol×28g/mol+3mol×2g/mol=62g,根据M=
计算其平均相对分子质量;
(3)该电池为燃料电池,交换膜为质子交换膜,说明溶液呈酸性,则负极上乙醇失电子发生氧化反应生成乙酸,正极上氧气得电子和氢离子反应生成水.
II.(1)该可逆反应是反应前后气体体积减小的放热反应,增大反应速率又有利于提高CO转化率,应该增大压强;
(2)该反应的正反应是放热反应,升高温度平衡向逆反应方向移动,则CO的转化率降低,所以Z表示最高温度下的反应;
a点时,n(H2)/n(CO)=1.5,反应开始时n(CO)=2mol,则开始时n(H2)=3mol,CO的转化率为50%,平衡时n(CO)=2mol×(1-50%)=1mol,n(H2)=3mol-2×(2mol×50%)=2mol,n(CH3OH)=1mol,平衡时混合气体的物质的量=1mol+2mol+1mol=4mol,混合气体质量=2mol×28g/mol+3mol×2g/mol=62g,根据M=
| m |
| n |
(3)该电池为燃料电池,交换膜为质子交换膜,说明溶液呈酸性,则负极上乙醇失电子发生氧化反应生成乙酸,正极上氧气得电子和氢离子反应生成水.
解答:
解:I.该反应中氧化过程为CuS→SO2,CuS作还原剂,要使该反应发生,需要氧化剂,酸性条件下KMnO4具有强氧化性,所以可以作氧化剂,则MnSO4为还原产物,溶液呈酸性,硫酸是反应物,水是生成物,根据转移电子相等、原子守恒配平方程式为6KMnO4+5CuS+14H2SO4=3K2SO4+6MnSO4+5CuSO4+5SO2↑+14H2O,
故答案为:6KMnO4+5CuS+14H2SO4=3K2SO4+6MnSO4+5CuSO4+5SO2↑+14H2O;
II.(1)该可逆反应是反应前后气体体积减小的放热反应,
A.随时将CH3OH与反应混合物分离,平衡向正反应方向移动,但反应速率不变,故错误;
B.降低反应温度平衡向正反应方向移动,但反应速率减小,故错误;
C.增大体系压强,平衡向正反应方向移动且反应速率增大,故正确;
D.使用高效催化剂,反应速率增大,但平衡不移动,故错误;
故选C;
(2)该反应的正反应是放热反应,升高温度平衡向逆反应方向移动,则CO的转化率降低,所以Z表示最高温度 270℃下的反应;
a点时,n(H2)/n(CO)=1.5,反应开始时n(CO)=2mol,则开始时n(H2)=3mol,CO的转化率为50%,平衡时n(CO)=2mol×(1-50%)=1mol,n(H2)=3mol-2×(2mol×50%)=2mol,n(CH3OH)=1mol,平衡时混合气体的物质的量=1mol+2mol+1mol=4mol,混合气体质量=2mol×28g/mol+3mol×2g/mol=62g,根据M=
得混合气体平均摩尔质量=
=15.5g/mol,气体的摩尔质量在数值上等于其相对分子质量,所以该混合气体的平均相对分子质量为15.50,
故答案为:270℃;15.50;
(3)该电池为燃料电池,交换膜为质子交换膜,说明溶液呈酸性,则负极上乙醇失电子发生氧化反应生成乙酸,电极反应式为CH3CH2OH+H2O-4e-=CH3COOH+4H+,正极上氧气得电子和氢离子反应生成水,电极反应式为O2+4H++4e-=2H2O,
故答案为:CH3CH2OH+H2O-4e-=CH3COOH+4H+.
故答案为:6KMnO4+5CuS+14H2SO4=3K2SO4+6MnSO4+5CuSO4+5SO2↑+14H2O;
II.(1)该可逆反应是反应前后气体体积减小的放热反应,
A.随时将CH3OH与反应混合物分离,平衡向正反应方向移动,但反应速率不变,故错误;
B.降低反应温度平衡向正反应方向移动,但反应速率减小,故错误;
C.增大体系压强,平衡向正反应方向移动且反应速率增大,故正确;
D.使用高效催化剂,反应速率增大,但平衡不移动,故错误;
故选C;
(2)该反应的正反应是放热反应,升高温度平衡向逆反应方向移动,则CO的转化率降低,所以Z表示最高温度 270℃下的反应;
a点时,n(H2)/n(CO)=1.5,反应开始时n(CO)=2mol,则开始时n(H2)=3mol,CO的转化率为50%,平衡时n(CO)=2mol×(1-50%)=1mol,n(H2)=3mol-2×(2mol×50%)=2mol,n(CH3OH)=1mol,平衡时混合气体的物质的量=1mol+2mol+1mol=4mol,混合气体质量=2mol×28g/mol+3mol×2g/mol=62g,根据M=
| m |
| n |
| 62g |
| 4mol |
故答案为:270℃;15.50;
(3)该电池为燃料电池,交换膜为质子交换膜,说明溶液呈酸性,则负极上乙醇失电子发生氧化反应生成乙酸,电极反应式为CH3CH2OH+H2O-4e-=CH3COOH+4H+,正极上氧气得电子和氢离子反应生成水,电极反应式为O2+4H++4e-=2H2O,
故答案为:CH3CH2OH+H2O-4e-=CH3COOH+4H+.
点评:本题考查较综合,涉及原电池原理、化学平衡计算、外界条件对化学平衡的影响、氧化还原反应等知识点,侧重考查学生分析问题、灵活运用知识解答问题能力,知道(1)中氧化剂的确定方法,了解常见的氧化剂、还原剂,题目难度中等.

练习册系列答案
 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
已知HI为无色气体,在一定条件下,对于可逆反应H2(g)+I2(g)═2HI(g),下列叙述中能表明该全品高考网“反应已达到化学平衡状态的是( )
| A、HI的生成速率与H2的生成速率相等 |
| B、H2的生成速率与I2的生成速率相等 |
| C、混合物的颜色不再发生变化 |
| D、H2、I2、HI的分子数之比为1:1:2 |
设NA为阿伏伽德罗常数的数值,则下列说法中不正确的是( )
①2.24L氖气含有NA个电子,
②18gD2O中所含的中子数为10NA,
③标准状况下,11.2LSO3 含有的分子数为0.5NA,
④过氧化钠与水反应,若电子转移2NA,则产生的氧气为32g,
⑤在1L 0.1mol/L的碳酸钠溶液中,CO32-总数小于0.1NA.
①2.24L氖气含有NA个电子,
②18gD2O中所含的中子数为10NA,
③标准状况下,11.2LSO3 含有的分子数为0.5NA,
④过氧化钠与水反应,若电子转移2NA,则产生的氧气为32g,
⑤在1L 0.1mol/L的碳酸钠溶液中,CO32-总数小于0.1NA.
| A、①②③⑤ | B、①④⑤ |
| C、①②③ | D、②③⑤ |
酒精灯的火焰分为三层,由外到内依次为外焰、内焰、焰心,若把一根洁净的铜丝,由外焰逐渐深入到内焰,能观察到的现象是( )
| A、始终是红色 |
| B、在外焰变为黑色,到内焰变为红色 |
| C、由红色变为黑色 |
| D、在外焰是红色,到内焰变为黑色 |
铜片放入热的稀硫酸中无明显现象,当加入下列哪种物质后现象有明显变化的是( )
| A、NaNO3 |
| B、HCl |
| C、NaOH |
| D、KCl |
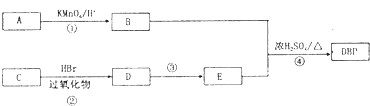 增塑剂是一种增加材料的柔软性或使材料液化的添加剂,不能用于食品、洒类等行业.DBP是增塑剂的一种,分子式为C16H22O4,可由常见的工业原料A(分子式为C8H10)和C合成DBP的路线如图所示:
增塑剂是一种增加材料的柔软性或使材料液化的添加剂,不能用于食品、洒类等行业.DBP是增塑剂的一种,分子式为C16H22O4,可由常见的工业原料A(分子式为C8H10)和C合成DBP的路线如图所示: